Tag: endokrynolog okulickiego
Peptyd C i cukrzyca
29 sierpnia, 2019 BlogBadanie peptydu C jest przydatne w obserwacji wydzielania insuliny i stawianiu diagnozy powodów niskiego poziomu glukozy we krwi czyli hipoglikemii. Oznaczenie peptydu C może być pomocne w ustalaniu, kiedy należy wdrożyć leczenie insuliną.

Poziom peptydu C to jeden z podstawowych wskaźników, które są stosowane do wyróżniania rodzajów cukrzycy. Po wykryciu cukrzycy typu 1 peptyd C wydaje sąd o czynności komórek beta wysp trzustkowych. Jeśli chodzi o cukrzycę typu 2 badanie peptydu C jest wskazówką, która mówi nam, że niezbędne będzie rozpoczęcie podawania egzogennej formy insuliny. W odniesieniu do peptydu C stosuje się określenie oceny rezerw wydzielniczych trzustki. Powstaje w równomolowych ilościach z insuliną. Do jego oznaczenia używa się próbki krwi.
Czym jest peptyd C?
Peptyd C jest wytwarzany w efekcie rozpadu proinsuliny. Jest to substancja składająca się z aminokwasów. Rozszczepianie łańcucha proinsuliny i uwalnianie peptydu C zostało omówione po raz pierwszy w 1967 roku. Procesowi temu towarzyszy powstawanie insuliny. Z uwagi na fakt, że obie te substancje produkowane są w takiej samej ilości- peptyd C jest uważany za jeden z najlepszych parametrów do oceny produkowania insuliny. Nie jest degradowany w wątrobie tak jak to się dzieje w przypadku insuliny. Na skutek tego utrzymuje się we krwi znacznie dłużej- czas półtrwania peptydu C to około 30 minut a insuliny – 5 minut. Sprawia to, że w krwioobiegu znajduje się zazwyczaj 5 razy więcej peptydu C niż insuliny. Jest to korzystne ponieważ za pomocą tego można określić ile insuliny zostało uwolnionej do krwi i wyprodukowanej przez trzustkę.
Do czego służy peptyd C?
Peptyd C jest przydatny nie tylko do określenia ilości insuliny wytwarzanej przez organizm, czyli endogennej, ale także róznicuje ją od insuliny egzogennej, czyli podawanej w postaci leku. W drugiej sytuacji nie zostaje wytwarzany peptyd C. Ważnym jego zadaniem jest rola kliniczna , którą odgrywa w różnicowaniu typu 1 i typu 2 cukrzycy oraz cukrzycy typu LADA. Standardy te, to znaczy wykorzystanie oceny stężenia peptydu C w diagnostyce diabetologicznej ma miejsce od 1973 roku.

Peptyd C zmniejsza zmiany chorobowe, które są następstwem cukrzycy typu 1, należą do nich: hiperfiltracja kłębuszkowa, demielinizacja neutronów i stan zapalny śrudbłonka naczyń. Podwyższa funkcjonalne i strukturalne właściwości nerwów obwodowych. Stanowi barierę przed indukowaną przez hiperglikemię apoptozę i aktywuje proliferację komórek nerwowych.
Badanie peptydu C w jakim celu się je wykonuje?
Badanie peptydu c wykonuje sie przede wszystkim, aby obserwować produkcje insuliny przez komórki beta wysp trzustkowych. Pomiar ten jest przydatny w poznaniu przyczyny hipoglikemii czyli niedocukrzenia. Niski poziom glukozy we krwi może być spowodowany na przykład nadmierną suplementacją insuliny, spożywaniem alkoholu, czy chorobami wątroby lub nerek.
Badania peptydu C stosuje się w celu monitorowania efektywności leczenia wyspiaka czyli guza trzustki, który przyczynia się do niekontrolowanego produkowania insuliny i peptydu C. Peptyd C może być pomocny przy hierarchizowaniu pacjentów do przeszczepu komórek wysp trzustkowych i obserwacji skuteczności leczenia po przeszczepie. Oznaczenie peptydu c jest przydatne w ocenie zagrożenia pojawienia się zespołu metabolicznego, czyli komponowaniu się z: nadciśnieniem tętniczym, otyłością brzuszną, podwyższonym poziomem glukozy we krwi, insulinoopornością i dyslipidemią.
Badanie peptydu C zalecane jest osobom chorym na cukrzycę. Wykonuje się je aby uzgodnić, czy potrzebne będzie wdrożenie terapii insulinowej, a także w przypadku podejrzenia insulinooporności. Chorzy, którzy przechodzą terapię insulinową mogą wytwarzać przeciwciała przeciwinsulinowe, które zwyczajowo interferują z wynikami oznaczeń insuliny. Jest to przeszkodą w określeniu stopnia wytwarzania insuliny endogennej. Wówczas oznaczenie peptydu C okazuje się niezawodną opcją dla badania poziomu insuliny.
Na czym polega badanie peptydu C?
Pożywką do badania peptydu C jest próbka krwi z żyły łokciowej. Zazwyczaj należy nie spożywać posiłków przez 8-10 godzin przed jej pobraniem. W dniu poprzedzającym badania wskazane jest wyeliminowanie z diety obfitych, tłustych posiłków i unikanie spożycia alkoholu. Tuż przed testem można wypić niewielką ilość wody.
Pobranie próbki na czczo ma na celu oznaczenie wyjściowego poziomu peptydu C. Pogłębioną charakterystykę możemy uzyskać po badaniu próbki z podaniem dożylnie glukagonu. Po 6 minutach ponawia się pobieranie krwi na oznaczenie peptydu C. Czeka się na odebranie wyniku średnio 10 dni. Za badanie trzeba zapłacić około 45 złotych.
Peptyd C interpretacja wyników
Określenia wyników badania peptydu C powinien dokonać specjalista. Wysokie stężenie substancji pojawia się w warunkach: zwiększonej produkcji insuliny endogennej, wysokiego stężenia glukozy we krwi, zespołu Cushinga, niewydolności nerek, hipokaliemii i podczas ciąży. Wysokie stężenia peptydu C może informować o wznowieniu wyspiaka lub obecności przerzutów. Z kolei jego niskie stężenie wskazuje na niewystarczające wytwarzanie insuliny endogennej i skuteczność leczenia wyspiaka.
Przy diagnozowaniu cukrzycy podwyższone stężenie peptydu C oznacza występowanie cukrzycy typu 2, a niskie cukrzycy typu 1. Bolączką jest także niskie stężenie peptydu C w surowicy nie zwiększające się popodaniu glukagonu, może ono świadczyć o obecności cukrzycy typu LADA, która zalicza się do cukrzycy typu 1 o wolno postępującym autoimmunologicznym procesie niszczenia komórek beta, występuje u dorosłych.
Normy dla peptydu C
Fizjolologicznie stężenie peptydu C na czczo powinno wynosić 0,2–0,6 nmol/l (0,7–2,0 μg/l), a w 6. minucie po podaniu glukagonu – 1–4 nmol/l. Jeżeli stężenie peptydu C zalicza się do normy oznacza to, że trzustka posiada odpowiednie rezerwy insuliny.
źródła zdjęć:
https://adst.mp.pl/img/articles/przeglad_badan/istock000026801375640x475.jpg
https://www.diabetes.org.uk/resources-s3/migration/older-women-321×221.jpg
https://www.zdrowiewpraktyce.pl/appFiles/site_162/images/newsFeed/JVWRA2Ia0OwUQFp.jpg
Zaburzenia rytmu serca u osób w podeszłym wieku
8 sierpnia, 2019 BlogMigotanie przedsionków – arytmia u osób starszych

Migotanie przedsionków jest najpopularniejszym zaburzeniem rytmu serca. Statystycznie aż 85% osób w wieku powyżej 65 lat cierpi na to zaburzenie. W formie trwałej migotanie przedsionków (AF) rzadko dotyczy zdrowego serca, dlatego standardowo występuje u osób starszych. Najczęściej zdarza się na skutek uszkodzenia serca przez wieloletnie ciśnienie tętnicze i chorobę niedokrwienną serca.
Objawy w postaci powikłań
Migotanie przedsionków może przebiegać bezobjawowo lub ujawnić się w postaci uczucia kołatania, czy szybkiego i niemiarowego bicia serca. Innymi symptomami mogą być zawroty głowy, omdlenia, osłabienie i poty. Aby wykryć tą chorobę należy wykonać badanie EKG, które pokazuje charakterystyczne cechy. Zazwyczaj wraz z tym badaniem powinno się wykonać również badanie obrazowe czyli echokardiograficzne. Wykazuje ono, czy serce jest zdrowe i czy ewentualnie nie doszło do powikłań choroby.

Najbardziej niebezpiecznym powikłaniem arytmii jest tworzenie się skrzepów krwi w sercu. Ponieważ ruch przedsionków nie przynosi rezultatów w przepychaniu krwi do komór, pozostaje ona w nich dłużej niż powinna, co powoduje procesy krzepnięcia (zgodnie z zasadą, że krew musi płynąć wartkim strumieniem, by pozostać płynną. Skrzeplina ma postać kruchą, łatwo ulegającą rozpadowi. W sytuacji, gdy fragment skrzepu dostanie się do naczyń, to wraz z prądem krwi przepłynie do mózgu, gdzie może pozbawić drożności mniejszej tętnicy, co odcina dalszy dopływ krwi i tlenu. Taki stan nazywamy udarem niedokrwiennym mózgu, którego następstwem może być śmierć lub trwałe inwalidztwo. Dlatego też ważne jest aby podjąć leczenie AF, choć może być ono z początku nieco uciążliwe.
Jak wygląda leczenie arytmii?
Leczenie składa się z kilku składników:
– U tej partii chorych, u których serce nie jest całkowicie zniszczone staramy się unormować stan pacjenta. Mówimy wówczas o kardiowersji. Na kardiowersję składa się podanie leku zwalczającego arytmię lub “porażenie” serca prądem z elektrod przyłożonych do skóry klatki piersiowej (podobnie jak to ma miejsce przy defibrylacji) i unormowaniu tym samym pracy serca.

– u chorych narażonych na szybki nawrot choroby, pilnujemy za pomocą leków, by serce pracowało w odpowiednim dle siebie rytmie. Takie postępowanie dobrze sprawdza się u chorych w starszym wieku z chorym sercem.
– niekiedy stosujemy leczenie zabiegowe zwane ablacją
– konieczne u wszystkich chorych jest leczenie przeciwzakrzepowe, czyli takie, które utrzymuje płynność krwi i nie dopuszcza do jej krzepnięcia. W większości przypadków sama aspiryna może okazać się niewystarczająca i należy wdrożyć leczenie tak zwanym doustnym antykoagulantem (Acenokumarol, Warfin). Leczenie musi być prowadzone pod ścisłym nadzorem ponieważ krew nie może być nadmiernie rozrzedzona, bo to grozi krwawieniami. Dlatego warto zwrócić się o pomoc lekarza, by ten kontrolował, czy zostały wykonane badania krwi przynajmniej raz w miesiącu.
źródła zdjęć:
http://www.bantamedia.com/wp-content/uploads/2016/01/The-Heart-of-the-Matter-Western-Health-Reserve-Heart-Health-Feature-old-woman-heart-635×450.jpg
https://cdn-prod.medicalnewstoday.com/content/images/articles/313/313217/chest-pain.jpg
https://clicktimez.com/wp-content/uploads/2016/10/cchat.jpg
Rola glukagonu w organizmie
16 lipca, 2019 BlogCzym jest glukagon?
Glukagon należy do hormonów polipeptydowych produkowanych i wydzielanych przez komórki wysp trzustkowych. W przeciwieństwie do insuliny, podwyższa on stężenie cukru we krwi. Można go nazwać hormonem “głodu” ponieważ jego wydzielanie jest zwiększone, gdy mamy dłuższe przerwy między posiłkami, a poziom cukru zaczyna się obniżać do wartości około 70 mg/dl.
Rola glukagonu w organizmie
Glukagon odgrywa ważną rolę w organizmie bo od niego zależą procesy kataboliczne, to znaczy, kiedy on działa organizm czerpie źródło energii z naszych wewnętrznych zapasów, które są magazynowane w wątrobie i tkance tłuszczowej. Dlatego też glukagon możemy nazwać hormonem od spraw spalania tkanki tłuszczowej.
Mechanizm działania glukagonu
Mechanizm działania glukagonu jest bardzo łatwy. Organizm zawsze chce zachować stan równowagi. Gdy stężenie cukru po posiłku jest wyższe, do działania włącza się insulina, która magazynuje glukozę z krwioobiegu w komórkach. Glukagon zaś stanowi przeciwny biegun.
W sytuacji, gdy długo nie spożywamy posiłku, a stężenie cukru we krwi zaczyna spadać, jest to bodziec dla trzustki, aby zaczęła wydzielać glukagon, który trafiając do wątroby zaowocuje przetworzeniem zgromadzonego w niej glikogenu do glukozy. Drugim miejscem, na który wpływ wywiera glukagon jest tkanka tłuszczowa. To właśnie dzięki glukagonowi zaczynamy przekształcać zapasy tłuszczu do glukozy. W ten sposób pozbywamy się niechcianych kilogramów tłuszczu i za jego sprawą utrzymujemy stabilny poziom glukozy we krwi.
Dodatkową pobudką do wytwarzania glukagonu przez trzustkę jest zwiększone stężenie aminokwasów we krwi, które jest następstwem spożycia przez nas produktów będących źródłem białka.
Glukagon i insulina
Glukagon i insulina to zbiór hormonów w naszym organizmie, które działają na prawidłową gospodarkę węglowodanów i tłuszczów. Ich wspólną rolą jest utrzymanie stężenia cukru we krwi w pewnych bezpiecznych wartościach (65 – 100 mg/dl). Wówczas czujemy się dobrze i nie mamy symptomów hiper- lub hipoglikemii.
Problem zaczyna się wtedy, gdy jeden hormon zaczyna górować nad drugim. W dzisiejszej rzeczywistości najbardziej doskwiera nam nadmiar insuliny. W sytuacji, gdy stężenie insuliny utrzymuje się na wysokim poziomie, cały czas jesteśmy nastawieni na “budowanie i gromadzenie zapasów”. Dlatego też powinno się zwrócić uwagę na odpowiednio dobraną dietę, która pomaga w regulacji wydzielania obu hormonów i dojściu do równowagi.
Nadmiar glukagonu i jego skutki
Bardzo rzadko przypuszcza się, że norma glukagonu została przekroczona. Lekarz może zalecić jego oznaczenie w badaniu biochemicznym, gdy istnieje podejrzenie między innymi: cukrzycy, guza trzustki lub dwunastnicy, bądź niewytłumaczalny ubytek masy ciała. Normalnie w warunkach laboratoryjnych glukagon powinien wynosić 50 – 100 ng/l. Kiedy jesteśmy na diecie wysokobiałkowej możemy sprawić, że w organizmie będzie wyższe stężenie tego hormonu, dlatego też mogą być wyższe wyniki we krwi.
Niedobór glukagonu i jego skutki
Niedobór glukagonu jest bardziej powszechny niż jego nadmiar. Możemy powiedzieć, że niedobór ten jest pozorny ponieważ jego powodem jest niewłaściwa dieta (taka, która zawiera łatwo dostępne węglowodany, dużo cukru oraz, gdy często podjadamy). W ten sposób tworzymy spiralę częstych i dużych wyrzutów insuliny.
Jeżeli zastosujemy badania oznaczania insuliny i glukozy na czczo, możemy wstępnie rozpoznać, czy koło napędzania insulinowego może być naszym udziałem. Według statystyk norma insuliny na czczo u zdrowej osoby wynosi ok. 3-6 iIU/m. Niepokojąca dla nas powinna być wartość insuliny na czczo w okolicach 10 – 12 uIU/m. Świadczy to o tym, że organizm wytwarza zbyt duże ilości tego hormonu, a zatem nie ma warunków aby zadziałał w naszym ciele glukagon. Takie osoby często cierpią z tego powodu, że trudno im schudnąć. Czesto można zauważyć u nich proces przybierania na masie ciała, niejako z powietrza.
Glukagon a odchudzanie
Glukagon jest niezwykle ważnym hormonem w odchudzaniu i znacznie ułatwia ten proces. To właśnie za sprawą jego produkcji przez trzustkę pobudzona zostaje tkanka tłuszczowa do zmiany kwasów tłuszczowych na energię. W sytuacji, gdy w organizmie dominuje insulina, glukagon nie może przeforsować swego działania. Osobom, u których zanotowano nadmierny wzrost insuliny zaleca się odpowiednie zestawienie produktów w diecie, w oparciu o te o niskim indeksie glikemicznym, oraz ustalenie pory posiłków.

Najbardziej minimalizuje produkcję glukagonu częste podjadanie. Kiedy robimy sobie przerwę na przekąskę, co dwie godziny, cały czas doprowadzamy do wydzielania insuliny. Wówczas glukagon jest nieprzydatny ponieważ dostarczamy energię z zewnątrz z której otrzymujemy glukozę nie ma więc potrzeby spalania własnych zapasów.
Trzeba pamiętać, że każda przegryzka (każdy orzeszek gryz jabłka, kromka chleba zjedzona w pośpiechu) jest bodźcem do wydzielania insuliny. Nawet kawa z mlekiem, którą pijemy w ciągu dnia łyk po łyczku jest odbierana przez nasz organizm jako przekąska. Dobroczynne może się okazać wydłużenie okresów bez jedzenia do około 3,5- 4 godzin, wówczas może zacząć działać glukagon.
To, co może zaowocować szybszym wydzielaniem glukagonu w okresie poposiłkowym to zawartość białka w spożywanym posiłku. A zatem posiłki, które bazują tylko na węglowodanach są mniej sprzyjające organizmowi.
Oto składniki, które powinny być obecne w diecie: warzywa, w postaci surowej i gotowanej, pełnoziarniste zboża (chleb razowy, gruba kasza na przykład pęczak), produkt będący dobrym źródłem białka (jajka, mięso, rośliny strączkowe, ryby, twaróg, jogurt naturalny), oraz dodatek tłuszczu (oliwa z oliwek, olej rzepakowy, orzechy, niewielki dodatek masła).
Owoce powinny znajdować się w diecie jednak w mniejszych ilościach niż warzywa. Optymalna dawka warzyw do owoców to 4:1. Owoce można z powodzeniem łączyć w posiłku z produktem białkowym (na przykład jogurt) i niewielkim dodatkiem tłuszczu (na przykład orzechy). Efektem tego będzie to, że unikniemy nagłego dużego skoku insuliny i spowodujemy szybsze wydzielanie glukagonu.
źródła zdjęć:
https://apteline-cms.azureedge.net/cdntypo3/_processed1_/e/c/csm_glukagon-model-struktura-molekularna-fotolia-m_e94414c28c.jpg
http://onkologia.org.pl/wp-content/uploads/trzustka.jpg
https://apteline-cms.azureedge.net/cdntypo3/_processed1_/f/a/csm_Monika_Frank_Dietetyk_4_ee9b2dc061.jpg
Obrzęk śluzowaty
25 lutego, 2019 BlogCzym jest obrzęk śluzowaty?
Obrzęk śluzowaty (ang. myxoedema ) kiedyś choroba Gulla. Można ją zaobserwować w niedoczynności tarczycy, która najczęściej ma formę choroby Hashimoto. Niedoczynność tarczycy może też pojawić się na skutek usunięcia gruczołu. Choroba ta może też być następstwem uszkodzenia przysadki lub braku, bądź niedostatecznego wydzielania podwzgórzowej tyreoliberyny, wówczas mówimy o postaci wtórnej. Występujące objawy choroby zależą od tempa rozwoju choroby oraz od wieku chorego.
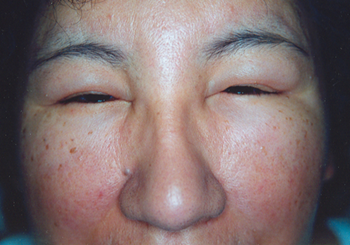
Obrzęk śluzowaty- przyczyny
Niedobór hormonów tarczycy ma wpływ na zmniejszenie podstawowej przemiany materii o około 35- 45%, co skutkuje umiarkowanym zmniejszeniem masy ciała (pomimo zmniejszonego łaknienia), małą odpornością na zimno i obniżeniem temperatury ciała. Do skutków spowolnienia procesów przemiany materii, należy obrzęk śluzowaty. Usytuowany on jest głównie w okolicach znacznego nagromadzenia tkanki łącznej wiotkiej -prowadzi to do pogrubienia rysów twarzy, obrzęków powiek, dłoni. Dochodzi do tego na skutek odkładania sie w tkance podskórnej fibronektyny i hydrofilnych glikozaminoglikanów, których synteza jest hamowana przez T3 (Trijodotyronina). Nieleczona niedoczynność tarczycy może stworzyć zagrożenie dla życia. Prowadzi do śpiączki w przebiegu obrzęku śluzowatego. Może go wywoływać już istniejąca choroba.
Obrzęk śluzowaty objawy
Poza obrzękiem występują objawy takie jak:
– znaczna bradykardia
– otępienie lub śpiączka
– hiponatremia
– hipotermia (<30 st.C, nawet do 24 st. C)
– hipoglikemia
– hipoksemia z hiperkapnią (spowodowana słabą wentylacją)
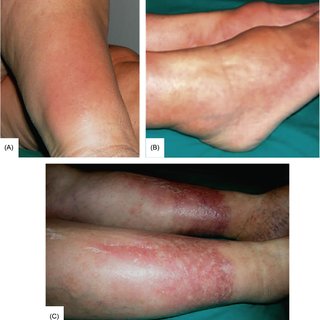
Rozwija się wstrząs. Mogą wystąpić drgawki mimo, że napięcie mięśniowe jest zmniejszone. Osłabione są także odruchy ścięgniste. Mogą pojawić się objawy przedmiotowe innych chorób współwystępujących (na przykład krwawienia z przewodu pokarmowego, zapalenia płuc lub innych zakażeń, zawału serca).
Zanim dojdzie do obrzęku śluzowatego pojawiają się objawy ostrzegawcze. Są to:
– zwiększenie stężenia białka C- reaktywnego (jeden z wykładników stanu zapalnego) oraz homocysteiny
– wzrasta stężenie cholesterolu całkowitego, frakcji LDL, trójglicerydów
– upośledzenie funkcji intelektualnych, pogorszenie pamięci
– ból głowy
– senność, spowolnienie
– czasem depresja
Najbardziej opresyjnymi objawami są zaburzenia funkcjonowania układu krążenia. Postępuje niewydolność skurczowa i rozkurczowa serca oraz typowo występująca bradykardia lub inne ciężkie zaburzenia rytmu serca. Zmniejsza się odporność na wysiłek, a w późniejszej fazie pojawia się niedoczynność wysięki w jamach opłucnowych, worku osierdziowym i otrzewnej.
W natężonej niedoczynności tarczycy może zostać uszkodzone wchłanianie jelitowe, czego przyczyną jest nawarstwianie w ich ścianach mukopolisacharydów. Symptomy choroby również mogą o sobie dać znać w funkcjonowaniu układu rozrodczego, pod postacią zaburzeń miesiączkowania, obniżenia libido, niebezpieczeństwa poronienia i porodu przedwczesnego, a także zaburzeń owulacji.
U mężczyzn również obserwuje się spadek libido zaburzenia erekcji. U 30-40% chorych postępuje niedokrwistość. Chorzy na niedoczynność tarczycy mogą się skarżyć na suchość skóry- skóra staje się pogrubiała i chłodna oraz zaczyna się łuszczyć. Może przybierać odcień sinawy lub żółty. Naruszona zostaje funkcja gruczołów łojowych i potowych. Typowym objawem jest także przerzedzenie owłosienia skóry głowy, wypadanie brwi, rzęs, utrata owłosienia płciowego.
Obrzęk śluzowaty- diagnostyka
Na diagnostykę niedoczynności tarczycy składają się badania: laboratoryjne, obrazowe, EKG. W badaniach krwi zauważa się zmniejszenie stężenia wolnych hormonów tarczycy, wzrost, prawidłowe lub zmniejszone TSH (odpowiednio do przyczyny) wysokie miano przeciwciał anty-TPO i anty- Tg (występuje w chorobie Hashimoto).
W przypadku śpiączki hipometabolicznej można zauważyć małe stężenia FT4, zwykle trochę powiększone TSH, zwiększenie stężenia cholesterolu, niedokrwistość, czasami hiponatremię i niewielką hiperkalcemię.
Bada się USG tarczycy – obraz w zależności od źródła niedoczynności tarczycy. W późnym stadium choroby USG jamy brzusznej może zdiagnozować płyn w jamie otrzewnej, RTG płuc- płyn w opłucnej i powiększenie sylwetki serca. W przypadku symptomów ze strony układu krążenia pomocne mogą się okazać EKG i echo serca.
Może się okazać, że niezwłocznie trzeba będzie wykonać scyntygrafię tarczycy. Kluczowe w rozpoznaniu śpiączki metabolicznej są objawy przedmiotowe przy wyeliminowaniu innych możliwych przyczyn śpiączki.
Obrzęk śluzowaty leczenie
Niedoczynność tarczycy leczy się podając suplementy hormonalne Tyroksynę (L-T4). Należy stosować się do zasady rozpoczynania leczenia od małych dawek, a potem stopniowego ich zwiększania. Przy odpowiednim dostosowaniu poziomu hormonalnego procesy metaboliczne ulegają przyspieszeniu i objawy powoli się wycofują.
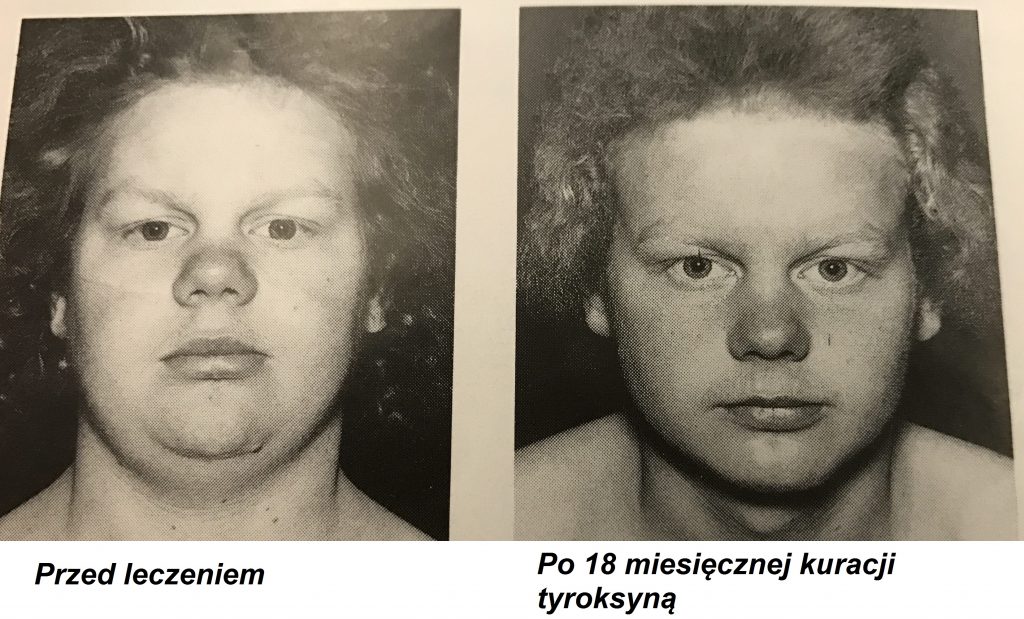
Leczenie śpiączki metabolicznej odbywa się na oddziale intensywnej terapii i jest zawsze wielopłaszczyznowe. Polega na przyjmowaniu L-T4 dożylnie, a kiedy zajdzie poprawa doustnie. Nie stosuje się tu zasady powolnego zwiększania dawki. Trzeba zapewnić odpowiednią wentylację płuc, wyrównanie stężeń elektrolitów i odpowiednią podaż płynów dożylnie. Wskazane jest leczenie chorób współwystępujących. Nie powinno się aktywnie ogrzewać chorego w hipotermii
źródła zdjęć:
Leptynooporność - ciągły głód i nadwaga?
5 lutego, 2019 BlogCo to jest leptyna i leptynooporność:
Leptyna wiąże się z otyłością. Za przyczyną leptyny pojawia się uczucie sytości. U osób otyłych często jej działanie jest upośledzone- może się tak dziać ze względu na występowanie zjawiska leptynooporności. Jej skutkiem może być to, że duże ilości leptyny zamiast hamować apetyt będą go pobudzały. Leptyna to białko zawierające w swojej cząsteczce 146 aminokwasów. Gen, który ma za zadanie syntezę leptyny nazwany został Ob – “ob”od angielskiego obese oznaczającego otyłość i zajmuje on u człowieka miejsce na chromosomie 7.
Najbardziej znana jest zależność pomiędzy leptyną, normalizowaniem apetytu oraz zawartością tkanki tłuszczowej. Białko to oddziaływuje również na wiele innych układów organizmu, na przykład na układ odpornościowy, układ rozrodczy, czy kostno- stawowy. Dla organizmu niekorzystny jest zarówno niedobór jak i nadmiar leptyny.
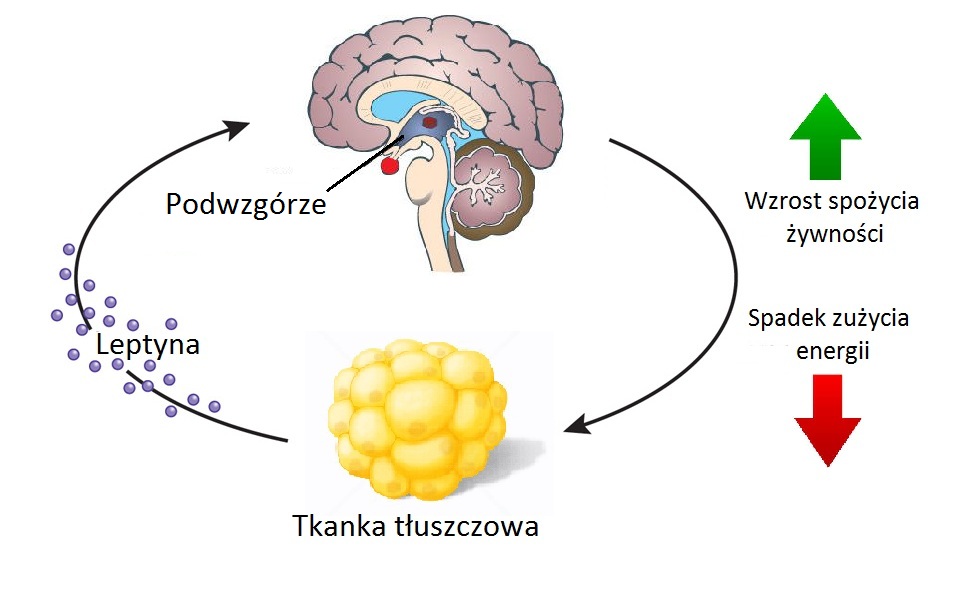
Leptyna produkcja hormonu
Leptyna jest produkowana przede wszystkim w białej (podskórnej) tkance tłuszczowej. Ilość wyzwalania hormonu łączy się z bezpośrednio z tym jak dużo tłuszczu dany człowiek magazynuje w ciele. U osoby z bardzo rozbudowaną tkanką tłuszczową zauważyć można wysokie stężenie leptyny w organizmie, z kolei u osób szczupłych ze względu na posiadanie niewiele tkanki tłuszczowej stwierdzić można niewielką ilość krążącej leptyny. U kobiet częściej zauważa się wyższe stężenie leptyny we krwi, z uwagi na fakt, że u tej płci naturalnie występuje większe nagromadzenie tkanki tłuszczowej.
Pochodzenie leptyny wywodzi się głównie z tkanki tłuszczowej. Jednak także inne tkanki ciała mają zdolność do uwalniania tego hormonu. W zdecydowanie mniejszych ilościach leptyna może być produkowana w:
– żołądku
– szpiku kostnym
– brązowej tkance tłuszczowej
– jajnikach
– łożysku
– mięśniach szkieletowych
Leptyna: leptynooporność i jej związek z otyłością
Leptyna jest nazywana hormonem sytości. Jak wyżej nadmieniono ilość leptyny w organizmie jest związana z rozmiarem tkanki tłuszczowej( im więcej tkanki tłuszczowej, tym więcej leptyny w organizmie). Zważywszy na to można by postawić tezę, że osoby otyłe nie odczuwają głodu. Dzieje się jednak odwrotnie.

Leptynoopornością nazywamy położenie, w którym mózg “nie reaguje” na leptynę. Etiologia leptynooporności jest nie do końca poznana. Przypuszcza się, że następstwem krążenia w organizmie wyjątkowo znacznych ilości leptyny jest zmniejszenie się ilości receptorów dla leptyny lub uszczuplenie ich odczuwania tego hormonu. Apetyt pozostaje niezaspokojony, kiedy organizm nie odbiera znaków o sytości. Problem pociąga za sobą konsekwencje mechanizmu błędnego koła. Im człowiek więcej je tym wzrasta jego poziom tkanki tłuszczowej. Występują anomalia ponieważ leptyna, która w normalnych warunkach powinna hamować apetyt jest źródłem odkładania się tłuszczu.
W wyniku leptynoodporności wzrastające ilości hormonu sytości jedynie podtrzymują tą patologiczną sytuację. Leptynooporność może wystąpić wtórnie czyli w wyniku rozwinięcia się u pacjenta nadwagi czy otyłości. Takie przyczyny leptynooporności są najczęstsze. Problemy z leptyną mogą stanowić zaburzenie o postaci pierwotnej. Przyczyna otyłości może pochodzić od mutacji genu dla leptyny. U takich pacjentów występuje nieposkromiony apetyt, przez co cierpią oni z powodu otyłości, z którą mogą się łączyć insulinoporność oraz zaburzenia płodności.
Można to uznać za nietypowe ale leptyna może być antagonistą odchudzania. Jeśli pacjent jest na diecie to redukcja kilogramów może prowadzić jak już wyżej wspomniano do spadku leptyny. Mechanizm odczuwania głodu wiąże się natomiast z leptyną. Im mniej tego białka znajduje się w organizmie tym większy odczuwamy głód. Zmiany ilości leptyny związane z dietą mogą stać się przyczyną efektu jo-jo.

źródła zdjęć:
https://calkiemzdrowo.pl/wp-content/uploads/2017/05/leptynooporność_3.jpg
https://i.sadistic.pl/pics/ca7f2c5a8248.jpg
https://wspbm.edu.pl/wp-content/uploads/2018/06/dietetyka.jpg
Niewydolność hormonalna jąder
21 stycznia, 2019 BlogCzym jest niewydolność hormonalna jąder?
Niewydolność hormonalna jąder nazywana jest również hipogonadyzmem lub hipogonadyzmem męskim pierwotnym. Zaburzenia występujące w okresie dojrzewania lub dojrzałości są przyczyną tej choroby. Wśród zaburzeń tych znajdują się np. zaburzenia jąder, komórek Sertoliego lub Leydiga. Do najczęściej spotykanych objawów tej choroby należą: bezpłodność, zmiana głosu męskiego na bardziej kobiecy, czy ginekomastię.
W leczeniu niewydolności hormonalnej jąder choremu podaje się głównie hormony- testosteron, jednak czasem konieczne jest usunięcie jednego jądra. Hipogonadyzm występuje w dwóch postaciach pierwotnej i wtórnej.
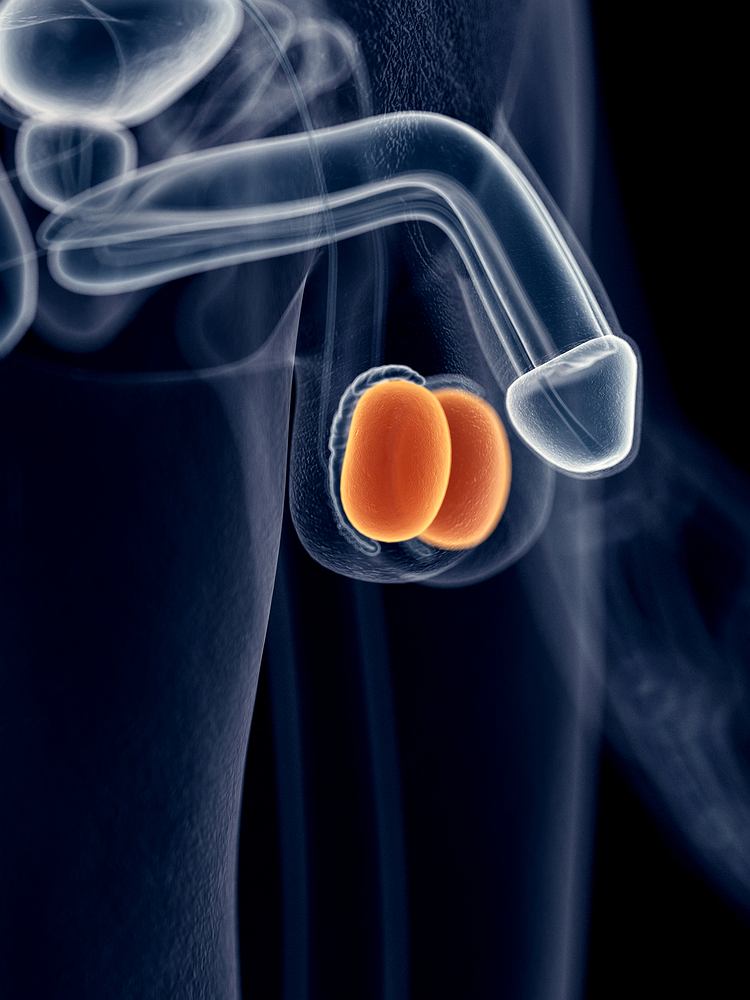
Jakie są rodzaje niewydolności hormonalnej jąder?
Niewydolność hormonalną jąder możemy podzielić na:
– całkowitą- wówczas równocześnie mamy do czynienia z niedoczynnością komórek Sertoliego oraz Leydiga (jest to spowodowane nadmiarem lutropiny i folitropiny)
– częściową- pojawia się zaburzona czynność hormonalna w komórkach Leydiga, następstwem tego jest nadmiar lutropiny lub brak czynności komórek Sertoliego
Przyczyny niewydolności hormonalnej jąder
Na niewydolność hormonalną jąder- przyczyniającą się m. in. do hipogonadyzmu- mogą wpływać różne czynniki takie jak:
– urazy mechaniczne
– promieniowanie Roentgena
– brak lub niedorozwój jąder (jądra)
– przewlekłe zatrucia (alkoholizm)
– choroby zakaźne ostre (rzeżączka, odra, ciągłe zapalenie przyusznic czyli świnka) i przewlekłe (kiła, gruźlica, cukrzyca)
– wiek (starzenie się)
– stany niedożywienia
– przepuklina pachwinowa
– wnętrostwo
– zaburzenie w chromosomach płciowych
– nowotwory
Nie ma ryzyka większych zaburzeń przy usunięciu lub uszkodzeniu jednego jądra w wypadku, gdy drugie jądro jest zdrowe. Zdrowe jądro przejmuje funkcje chorego.
Pierwotna niewydolność hormonalna jąder- jej przyczyny należy szukać w samych jądrach.
Wtórna niedoczynność hormonalna jąder- zachodzi gdy jądra zostają bezpośrednio uszkodzone na skutek zaburzeń w wydzielaniu hormonów (podwzgórza czy przysadki).
Eunuchoidyzm a niewydolność hormonalna jąder – różnice
Zespół objawów, który jest spowodowany niedorozwojem lub niedoczynnością jąder nazywany jest eunuchoidyzmem. Są uzależnione od wieku.
Możemy wówczas zauważyć:
– owłosienie i wygląd skóry typu kobiecego
– zmniejszenie siły mięśniowej
– niedorozwój narządów płciowych
– bezpłodność
– nadmiernie wysoki wzrost
– zanik mięśni
– zmęczenie
– brak wzwodu
– wysoki ton głosu
– zmniejszenie popędu płciowego
– brak mutacji
Nasilenie wymienionych objawów jest odpowiednio dostosowane do stopnia niedoczynności jąder. Kiedy jedno jądro jest zdrowe, to usunięcię drugiego nie ma wpływu na pojawienie się szczególnych zaburzeń w organiźmie.
Niewydolność hormonalna jąder – diagnoza i leczenie
Rozpoznanie choroby odbywa się na podstawie objawów, a także biorąc pod uwagę wyniki badań chorego. Po analizie wyników badań lekarz dokonuje diagnozy.
Do potrzebnych badań, które trzeba wykonać należą: badania hormonalne LH i FSH oraz badania prolaktyny, USG jąder i badania morfologiczne. Obejmują one (badania) sprawdzanie poziom hormonów męskich – androgenów (głównie testosteronu).

Jeśli chodzi o kwestię leczenia to pacjent powinien przyjmować preparaty z hormonami głównie z testosteronem przez odpowiednio długi czas. Leczenie takie określa się jako substytucyjne. Terapia odbywa się jedynie w specjalistycznych placówkach, biorąc pod uwagę całokształt stwierdzonych zmian – głównie laboratoryjnych badań hormonalnych.
źródła zdjęć:
Jedna z przyczyn niepłodności - Hiperprolaktynemia
7 stycznia, 2019 BlogHIPERPROLAKTYNEMIA
1. Co to jest hiperprolaktynemia?
Hiperprolaktynemia to podwyższony ponad stan normy poziom prolaktyny w surowicy krwi. Prolaktyna jest hormonem dostarczanym przez przysadkę mózgową. Od tego hormonu zależy przede wszystkim wzrost płodu, a także gruczołów sutkowych w czasie ciąży. Po porodzie uaktywnia laktację. Mamy mogą karmić swoje dzieci właśnie za sprawą wysokiej prolaktyny. Hormon ten odpowiada także za inne zadania takie jak: wpływ na układ odpornościowy, bierze też udział w reakcji stresowej organizmu.
Prawidłowe stężenie prolaktyny u kobiet to:< 23 µg/l w fazie folikularnej (czyli początkowej fazie cyklu miesiączkowego zaczynającej się w pierwszym dniu miesiączki) i < 40 µg/l w fazie lutealnej (czyli w okresie poprzedzającym wystąpienie miesiączki), u mężczyzn natomiast < 20 µg/l. O hiperprolaktynemii mówimy gdy wartości te są znacznie wyższe.

2. Hiperprolaktynemia objawy
Objawami, których nie należy lekceważyć są: drażliwość, złe samopoczucie, nawracające bóle głowy, zaburzenia miesiączkowania czy wręcz wtórny zanik miesiączki, stany depresyjne, kłopoty z cerą, otyłość, ból piersi, trądzik, nadmierne owłosienie, mlekotok, ginekomastia (u mężczyzn). Wraz z występowaniem tych objawów prolaktyna osiąga poziom nawet 50 µg/l.
3.Hiperprolaktynemia przyczyny
Przyczyny fizjologiczne hiperprolaktynemii to ciąża i okres karmienia piersią. Zaobserwowano wzrost prolaktyny także podczas drażnienia brodawek sutkowych oraz stymulacji szyjki macicy- czyli podczas stosunku płciowego- podczas snu, po zjedzeniu potrawy bogatej w białko, a także podczas wysiłku fizycznego.
Wskaźniki patologiczne wywołujące hiperprolaktynemię to te, których powinien szukać lekarz. Najczęstszym sprawcą choroby są leki działające na układ nerwowy, przeciwdepresyjne. Następnie należy wspomnieć o takich przyczynach jak niedoczynność tarczycy i kory nadnerczy.
Czynnikami podwyższającymi prolaktynę są także: stres, choroby obejmujące ścianę klatki piersiowej, jak na przykład półpasiec, następnie gruczolaki (guzki) przysadki mózgowej, a także inne guzy naciskające na przysadkę mózgową, niewydolność i nowotwór nerek, rak oskrzeli, marskość wątroby. Te ostatnie przyczyny spotykane są rzadko. Niektórzy naukowcy głoszą, że winowajcami choroby są głównie leki psychotropowe. W Polsce za chorobę odpowiedzialny jest szeroko rozumiany stres psychiczny i fizyczny. Jest on bowiem przyczyną wzrostu wydzielania w organiźmie β-endorfin, które zwiększają aktywność opioidową mózgu i podwzgórza , czego następstwem jest wzrost wydzielania prolaktyny.
4. Hiperprolaktynemia leczenie
Hiperprolaktynemia sama w sobie nie stanowi choroby, a jedynie jest objawem jakiejś choroby, którą należy leczyć. Kiedy mówimy o podniesionym poziomie prolaktyny nie mamy na myśli diagnozy, ale punkt wyjścia do dalszych badań.

Aby wybrać sposób leczenia hiperprolaktynemii należy poznać jej przyczynę. Warto poddać się kontroli kompetentnego lekarza, który dokona selekcji leków zażywanych przez pacjenta w sposób ciągły oraz wykluczy podejrzenie innych chorób takich jak niedoczynność tarczycy. Jeżeli pacjent przyjmuje leki na przykład przeciwdepresyjne, to lekarz wspólpracując z psychiatrą może zalecić ich odstawienie na 2-3 dni i wówczas dokonać pomiaru poziomu prolaktyny. Gdy okaże się, że farmaceutyki są przyczyną wzrostu poziomu tego hormonu, konieczna może okazać się zmiana leków.
Gdy istnieje przypuszczenie guza przysadki lekarz powinien zadbać o skierowanie pacjenta na MRI głowy. Z uwagi na dobrą reakcję na leczenie farmakologiczne i zmniejszanie się gruczolaków po zastosowaniu leków nie usuwa sie ich chirurgicznie. Są wdrażane leki z grupy agonistów receptorów dopaminergicznych- do ich funkcji należy zahamowanie wydzielania prolaktyny.
Lekarze stosują następujące farmaceutyki:
– cabergolina (Dostinex)- jest najdroższy ale nie powoduje skutków ubocznych. Można go zażywać tylko 2 razy w tygodniu a nawet rzadziej.
– quinagolid (Norprolac)
– bromokryptyna (Parlodel, Bromergon, Bromocorn) – jest lekiem niedrogim ale powoduje wiele skutków ubocznych.
źródła zdjęć:
https://cdn-images-1.medium.com/max/120/1*Fz4m6niguHG1UeTwbOjynQ.jpeg
http://nextews.com/images/59/9a/599a0c6d7df70ec9.jpg
https://plodnosc.pl/wp-content/uploads/2018/10/Fotolia_153393112_Subscription_Monthly_M-420×292.jpg
Choroba Hashimoto
28 września, 2018 BlogChoroba Hashimoto określana jest też mianem- przewlekłe limfocytarne (autoimmunologiczne) zapalenie tarczycy. Pierwszy raz informacje o chorobie Hashimoto zostały opublikowane przez japońskiego lekarza Hakaru Hashimoto w 1912 roku. Choroba Hashimoto ma charakter choroby z autoagresji. Polega ona na tym, że w układzie immunologicznym (odpornościowym) następuje błąd. Skutkuje to tym, że organizm zwraca się przeciwko sobie. Białka tarczycowe są identyfikowane przez organizm jako wrogie. Układ immunologiczny niszczy je, co sprawia że upośledzona jest aktywność enzymu odpowiedzialnego za syntezę hormonów tarczycy.
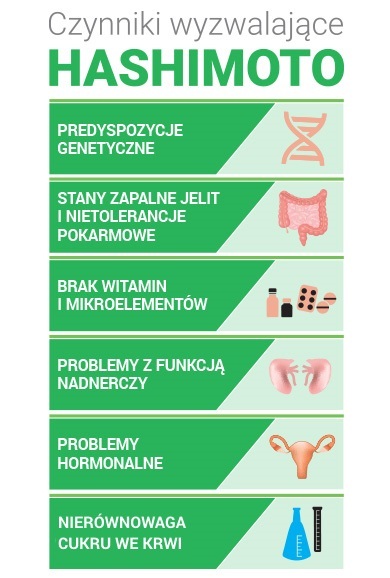
Choroba Hashimoto przyczyny powstawania:
Szczególnie narażone na zachorowanie są osoby z cukrzycą typu 1, a także te u których w rodzinie ktoś chorował na tarczycę. Zdarzają się przypadki, że matka ma chorobę Gravesa- Basedowa, która powoduje nadczynność tarczycy, a córka cierpi na hashimoto, co wywołuje u niej niedoczynność tarczycy. Zazwyczaj autoimmunologiczne zapalenie tarczycy jest rodzinne. Do zachorowania na tę chorobę mogą się przyczynić także: przewlekły stres, problemy psychiczne, przemęczenie lub infekcja- ponieważ powodują one osłabienie odporności. Hashimoto często pojawia się u kobiet niedługo po porodzie. Wtedy często przechodzi w stan ukryty, by wcześniej czy później znów powrócić. U co drugiej osoby może to skutkować trwałą niedoczynnością tarczycy.
Choroba Hashimoto objawy:
W toku choroby objawy mogą się nie ujawniać. Osoba z hashimoto może nie mieć świadomości choroby. W niektórych przypadkach tarczyca jest zmieniona zapalnie, stopniowo się powiększa tworząc wole. Ma postać twardą, spoistą i nierówną. Rzadko występuje ból przy dotyku i tylko czasami daje uczucie pełności lub ucisku gardła. Choroba Hashimoto może mieć postać zaniku tarczycy. Początkowo praca tarczycy jest prawidłowa-wydziela odpowiednią lub nadmierną ilość hormonów. Po wielu miesiącach lub latach ewoluuje niedoczynność, która pogarsza zdrowie.
W hashimoto występują objawy niespecyficzne:
-senność
-zmienność nastrojów
-obfite miesiączki
-marznięcie
-kłopoty z koncentracją i pamięcią
-suchość i szorstkość skóry
-skłonność do depresji
-zaparcia
-podwyższony poziom cholesterolu
-bóle mięśni i stawów
-nieuzasadnione tycie
-wypadanie włosów
Powyższe objawy nie muszą jednak świadczyć o chorobie.
Choroba Hashimoto leczenie:
Leczenie polega na terapii skutków nie przyczyny choroby- ponieważ nie ma leku, który skutecznie powstrzymałby błąd w działaniu układu odpornościowego odpowiedzialny za rozwój choroby. Kontrolne badania powinno się wykonywać i są wystarczające, kiedy we krwi stwierdzono przeciwciała ale tarczyca nie jest powiększona i pracuje prawidłowo. Jeżeli zdiagnozowano niedoczynność trzeba zażywać syntetyczne preparaty tyroksyny wyrównujące poziom hormonów tarczycy we krwi. Większość chorych musi przyjmować leki do końca życia. Ze względu na to że poziom niedoczynności jest zmienny, pacjent powinien mieć dawki leków ustalone przez lekarza i podlegać jego kontroli. Preparat przyjmuje się raz dziennie na czczo pół godziny przed śniadaniem i innymi lekami, wtedy wykazuje najlepszą wchłanialność.
Czasami choroba może samoistnie ustąpić, wówczas pacjent może odstawić leki. Dzieje się tak głównie u dzieci, osób młodych, z zapaleniem poporodowym. Choroba jednak może powrócić bo przeciwciała mogą zaatakować w każdej chwili. Dlatego osoba chora na hashimoto powinna być pod stałą opieką lekarską bez względu na przebieg choroby.

Specjalizacją, która zajmuje się leczeniem tego schorzenia jest endokrynologia. W naszej Przychodni, która znajduje się na ulicy Okulickiego w ramach tej specjalizacji przyjmuje lek. med. Anna Fedorowicz. W celu zarejestrowania się do tego lekarza lub innych specjalistów przyjmujących w naszej przychodni mogą Państwo skorzystać z rejestracji online, znajdującej się pod adresem: www.bjmedical.pl/rejestracja
Źródła zdjęć:
Andropauza
22 czerwca, 2018 BlogAndropauza występuje u mężczyzn. Mówimy o niej wtedy, gdy mężczyzna wchodzi w wiek po 50 roku życia, zapowiadający zbliżający się okres starości. Andropauza łączy się z szeregiem dolegliwości odpowiadających temu wiekowi.
Objawy andropauzy:
U mężczyzn występują następujące objawy andropauzy czyli przekwitania:
jest wyczuwalna nadmierna potliwość, napady gorąca i zaburzenia snu porównywalne do tych, które towarzyszą kobietom w trakcie menopauzy,
ogólna wydolność organizmu zostaje obniżona ze względu na postępującą miażdżycę naczyń krwionośnych. Pacjent ma trudności takie jak zadyszka przy wejściu na trzecie piętro, czy po biegu na autobus,
są obecne kłopoty z pełnym wzwodem, które wiążą się ze zmianami naczyniowymi czy z obniżeniem poziomu hormonów. Może dojść do impotencji,
pojawia się nadmierna wrażliwość, częsta zmiana nastrojów, pacjent może popaść w depresję. Może się to objawiać agresją u niektórych mężczyzn,
można zaobserwować nagromadzenie na brzuchu tkanki tłuszczowej,
czasami dochodzi do kłopotów z oddawaniem moczu, co jest następstwem przerostu gruczołu krokowego
pacjent może odczuwać bóle kręgosłupa, mogą być one utożsamiane ze zmianami zwyrodnieniowymi, problemem jest natomiast osteoporoza, która tak jak u kobiet ma tło hormonalne i poddaje się leczeniu.
Andropauza przyczyny:
Pacjent cierpiący na inne choroby jest bardziej podatny na wystąpienie objawów andropauzy. Obecność andropauzy jest bardziej uzależniona od ogólnej kondycji mężczyzny niż od wieku. Rozwój męskiego przekwitania może być szybszy, kiedy występują takie dolegliwości jak: cukrzyca, miażdżyca, nadciśnienie ale również nadużywanie alkoholu, palenie papierosów, mało aktywny tryb życia, złe odżywianie się (np. dieta zbyt bogata w tłuszcze zwierzęce). Mówiąc o pierwszych objawach andropauzy należy brać także pod uwagę uwarunkowania genetyczne; jeżeli u ojca pojawiły się wcześnie może być tak też u syna.
Andropauza skutki:
Organizm wydziela mniej hormonów po 50 roku życia wtedy też najczęściej występują pierwsze objawy przekwitania u mężczyzn. Zmniejsza się produkcja testosteronu przez jądra oraz wydzielanie androgenów DHEA przez nadnercza, hormonu wzrostu przez przysadkę mózgową i melatoniny przez szyszynkę. W organizmie zachodzą zmiany. Niedobór testosteronu skutkuje obniżeniem popędu płciowego i zaburzeniem erekcji. Następstwem deficytu męskiego hormonu może też być pogorszenie sprawności fizycznej i psychicznej. Spadek DHEA powoduje zmniejszenie wydajności organizmu i pogorszenie samopoczucia. Niski poziom hormonu wzrostu przyczynia się do spadku zdolności organizmu do szybkiej regeneracji. Występują duże problemy z przemianą materii oraz wypróżnieniami. Mężczyźni coraz częściej uskarżają się na bezsenne noce z powodu spadku melatoniny.
Andropauza leczenie:
W celu złagodzenia skutków andropauzy stosuje się leczenie hormonalne. Podczas tej terapii uzupełnia się poziom męskiego hormonu testosteronu. Leczenie to powinno przynieść takie rezultaty jak: obudzenie popędu płciowego, poprawa samopoczucia, wzmocnienie kości i mięśni. Dla wzmocnienia skutków terapii ważna jest też zmiana stylu życia. Pomocne może się okazać zwiększenie aktywności fizycznej oraz odpowiednia dieta, unikanie smażonych i tłustych potraw, papierosów, alkoholu. Zdrowy tryb życia zapewnia opóźnienie procesów starzenia się.

Specjalizacją, która zajmuje się leczeniem tego schorzenia jest endokrynologia. W naszej Przychodni, która znajduje się na ulicy Okulickiego w ramach tej specjalizacji przyjmuje lek. med. Anna Fedorowicz. W celu zarejestrowania się do tego lekarza lub innych specjalistów przyjmujących w naszej przychodni mogą Państwo skorzystać z rejestracji online, znajdującej się pod adresem: www.bjmedical.pl/rejestracja
Źródła zdjęć:
http://slideplayer.pl/slide/1281392/
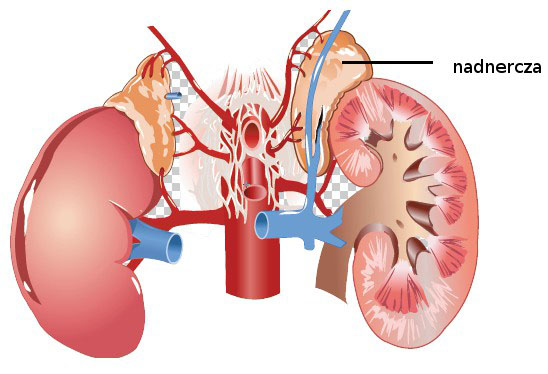
Nadczynność i niedoczynność nadnerczy
11 maja, 2018 BlogNadczynność i niedoczynność nadnerczy są chorobami kory nadnerczy. Pierwsze z wymienionych schorzeń charakteryzuje się zmniejszonym wydzielaniem nadnerczowych hormonów steroidowych, drugie objawia się obecnością guza chromochłonnego.
Nadczynność i niedoczynność nadnerczy przyczyny:
Wyróżniamy niedoczynność wtórną i pierwotną nadnerczy. Przyczyną niedoczynności wtórnej jest nieprawidłowa funkcja przysadki natomiast na niedoczynność pierwotną ma wpływ uszkodzenie nadnerczy. Wtórną odmianę tej choroby możemy zdiagnozować u około 60% pacjentów.
Do głównych przyczyn niedoczynności pierwotnej nadnerczy zaliczamy:
gruźlicę
autoimmunologiczne zapalenie kory nadnerczy
Charakterystyczne przyczyny wtórnej niedoczynności nadnerczy to:
urazy oraz guzy w okolicy podwzgórzowo-przysadkowej
długotrwałe stosowanie glikokortykosteroidów w dużych dawkach
Nadczynność nadnerczy powodują:
pierwotna choroba nadnerczy
samoistna nadczynność nadnerczy (zbyt duża ilość kortyzolu jest produkowana samoistnie przez gruczoł)
nowotwór przysadki
zespół Cushinga-który jest wywołany rzadką wadą genetyczną co skutkuje większym ryzykiem zachorowania na raka gruczołów endokrynnych
nowotwór ektopowy produkujący ACHT
nowotwór zwany ektopowym, którego cechą jest nieprawidłowe umiejscowienie gruczołu wytwarzającego hormon, mimo to jest on czynny i wytwarza kortyzol
Objawy nadczynności i niedoczynności nadnerczy:
U pacjentów z nadczynnością nadnerczy mogą występować:
zaniki i osłabienie mięśni
wysokie ciśnienie tętnicze krwi
bóle kostne
zaburzenia miesiączkowania
trądzik
łysienie typu męskiego
powiększenie łechtaczki
może występować utajona lub jawna cukrzyca
Oprócz tych objawów mogą występować charakterystyczne zmiany w wyglądzie zewnętrznym oraz w wyglądzie skóry takie jak: otyłość dotycząca tułowia i karku z zachowaniem szczupłych kończyn, zaokrąglona twarz, różowe rozstępy skórne podbrzusza, bioder, ud i sutków.
Do głównych objawów niedoczynności nadnerczy zaliczamy:
nudności
wymioty
ból brzucha
osłabienie
większa ochota na słone potrawy
hipoglikemię czyli małe stężenie glukozy we krwi
obniżenie masy ciała
zmęczenie
brak apetytu, zaciemnienie skóry- choroba Addisona
niskie ciśnienie
- bladość skóry-wtórna niedoczynność kory nadnerczy
Leczenie nadczynności i niedoczynności nadnerczy
Niedoczynność kory nadnerczy leczy się uzupełniając brakujące hormony. W przypadku pierwotnej niedoczynności zaleca się używanie glikokortykosteroidów lub androgenów, najczęściej jednak stosuje się mineralokortykosteroidy. Przy leczeniu wtórnej niedoczynności mogą okazać się pomocne glikokortykosteroidy oraz androgeny.
Specjalizacją, która zajmuje się leczeniem tego schorzenia jest endokrynologia. W naszej Przychodni, która znajduje się na ulicy Okulickiego w ramach tej specjalizacji przyjmuje lek. med. Anna Fedorowicz. W celu zarejestrowania się do tego lekarza lub innych specjalistów przyjmujących w naszej przychodni mogą Państwo skorzystać z rejestracji online, znajdującej się pod adresem: www.bjmedical.pl/rejestracja
Źródła zdjęć:
http://zycie.ca/niedoczynnosc-nadnerczy-czyli-recepta-na-katastrofe/

