Tag: neurolog Nowa Huta
Narkolepsja
20 września, 2019 BlogCo to jest narkolepsja?
Narkolepsja należy do chorób neurologicznych. Jej istotą jest nadmierna senność w ciągu dnia. Za jej etiologię uważa się niedobór hipokretyny- białka, które jest odpowiedzialne za regulowanie snu i czuwania. Zmniejszona produkcja hipokretyny jest skutkiem uszkodzenia bocznego podwzgórza (część mózgu), od którego uzależniony jest sen. Powszechnie głoszą, że dzieje się tak w wyniku nieprawidłowej reakcji układu odpornościowego, którą wywołuje banalna infekcja.

Narkolepsja cztery główne objawy
Nie zawsze występują wszystkie cztery objawy w toku choroby.
– senność, która występuje w ciągu dnia- Ten objaw jest pierwszym, a czasami jedynym symptomem choroby. Chorym zdarza się zasypiać w czasie krótszym niż 5 minut w przypadkach, gdy zdrowa osoba jest aktywna, na przykład podczas rozmowy z przełożonym. Senność zmienia się w ciągu dnia. Po krótkiej drzemce ustępuje, po czym znów się nasila.

– katapleksja-Jest to objaw, który występuje wyłącznie w narkolepsji. Katapleksja polega na spadku napięcia mięśniowego w sytuacjach emocjonalnych (np. gniew, śmiech). Za sprawą zwiotczenia mięśni chorzy miękko osuwają się na ziemię. Kiedy uszkodzenie podwzgórza jest niewielkie wiotczeją jedynie mięśnie twarzy, co przejawia się bełkotliwą mową i opadającą żuchwą.
– halucynacje senne -Narkolepsja łączy się z fazą snu REM, w której występują marzenia senne. Faza non- REM (głęboka, bez snów) powinna poprzedzać fazę REM tak jak to się dzieje u osób zdrowych. Narkolepsja charakteryzuje się tym, że chorzy na nią zapadając w sen od razu zagłębiają się w świat bardzo rzeczywistych marzeń sennych, które zazwyczaj budzą lęk i są podobne do halucynacji.
– paraliż przysenny– występuje podczas zasypiania albo tuż po obudzeniu. Pojawia się niemożność poruszania się przez kilka lub kilkanaście sekund ponieważ ciało jest sparaliżowane tak jak w czasie marzeń sennych, jednak świadomość nie jest uśpiona.
Narkolepsja – diagnoza
W postawieniu trafnej diagnozy pomagają badania snu pacjenta w nocy i w ciągu dnia (czujniki zapisują na przykład liczbę drzemek, zasypianie od razu fazą snu REM). Innym sposobem na rozpoznanie choroby jest pobranie płynu mózgowo- rdzeniowego oraz sprawdzenie poziomu hipokretyny, w Polsce jednak nie stosuje się tego sposobu.
Narkolepsja – leczenie

Aby wyleczyć katapleksję i halucynacje wdraża się leczenie przeciwdepresyjne natomiast na nadmierną senność stosuje się preparat używany w terapii ADHD- nie zawsze jednak wykazuje on skuteczność. Na świecie rozpowszechniony jest inny lek działający pobudzająco. Ma on właściwości stymulujące dzięki którym pacjent może w miarę normalnie funkcjonować nie zapadając w drzemkę w ciągu dnia. Kiedy przypadek jest ciężki do leczenia włącza się hydroksymaślan sodu, który ułatwia dobry sen nocą i ogranicza ataki snu w dzień. Niestety oba wspomniane wyżej leki nie podlegają refundacji, a indywidualny ich import jest kosztowny.
źródła zdjęć:
- https://www.therecoveryvillage.com/wp-content/uploads/2018/11/NARCOLEPSY.jpg
- https://www.kobieta.pl/media/cache/default_view/uploads/media/default/0001/53/a71373299f28a02003e63324df9e775a7b189bd5.jpg
- https://media.healthday.com/Images/icimages/doc_teen2262.jpg
Encefalopatia Wernickiego
30 lipca, 2019 BlogCo to jest zespół Wernickiego- Korsakowa?
Zespół Wernickiego to choroba o podłożu neurologicznym, której źródłem jest niedobór witaminy B1 czyli tiaminy. Kiedy jesteśmy zdrowi niedobór tiaminy jest bardzo rzadki. Najczęściej zespół Korsakowa spotyka się u osób przewlekle nadużywających alkohol. W tej chorobie możemy wyróżnić objawy neurologiczne i psychiatryczne. Głównie występują zaburzenia świadomości, rytmu dobowego, konfabulacje. Choroba ta zalicza się do zespołu objawów z grupy zaburzeń psychiatrycznych.
Zespół niedoboru witaminy B1
Witamina ta- tiamina należy do grupy witamin B. Tiamina występuje powszechnie w składzie wielu produktów roślinnych i zwierzęcych. Bogate są w nią głównie zboża (szczególnie bez wysokiej obróbki mechanicznej), rośliny strączkowe oraz mięso. Klasyczna dieta nie powoduje niedoboru tiaminy poniewż występuje ona powszechnie.

Do zmniejszenia jej stężenia w organizmie mogą doprowadzić schorzenia, które przebiegają z zaburzeniami wchłaniania. Wśród nich można wymienić:
– bulimię
– anorexię nervosę
– choroby żołądka
– raka żołądka
– zespół krótkiego jelita
Najpowszechniej jednak niedobór tej witaminy ma związek z nadużywaniem alkoholu.
Objawy zespołu Wernickiego
Występujący z pełnymi objawami zespół niedoboru witaminy B1 nazywany jest w terminologii medycznej zespołem Wernickiego – Korsakowa. Zespół ten składa się z objawów neurologicznych oraz psychiatrycznych. Trzeba pamiętać, że w zespole Wernickiego objawy psychiatryczne różnią się, tak przebiegiem jak i rodzajem, od tych które są obecne w zespole Korsakowa. Dodatkowymi skutkani ubocznymi niedoboru tiaminy są zaburzenia ze strony krążenia oraz zmiany skórne.
Zgodnie z nazwą zespół Wernickiego- Korsakowa sklada się z dwóch części – z zespołu Wernickiego i zespołu Korsakowa.
Klasycznie objawy w zespole Wernickiego pojawiają się w sposób gwałtowny. Często objawy mogą występować po wcześniejszym nadmiernym spożyciu cukrów. Statystycznie, kiedy nie jest objęty leczeniem nawet w 60% prowadzi do zgonu.
Objawy zespołu Wernickiego możemy sklasyfikować jako -objawy psychiatryczne oraz neurologiczne.
Do tych pierwszych możemy przypisać:
– zaburzony rytm dobowy- najbardziej typowe jest znaczne pobudzenie w godzinach nocnych
– zaburzenia świadomości pod postacią splątania, czasem prowadzące do śpiączki. Człowiek jest pozbawiony poczucia czasu, tego jak się nazywa, pory roku, nie umie określić, gdzie mieszka.
– obecny jest oczopląs (szybkie ruchy gałek ocznych w jednym kierunku) zaburzenie skojarzonego spojrzenia gałek ocznych oraz upośledzona reakcja źrenic na światło
– wśród zaburzeń neurologicznych głównie możemy wymienić zaburzenia gałkoruchowe oraz zaburzenia postawy nazywane ataksją tułowia, której przejawem jest niemożność utrzymania prawidłowej postawy ciała.
Z uwagi na fakt, że witamina B1 jest konieczna do prawidłowego funkcjonowania układu krążenia, jej niedobór w zespole Wernickiego może przyjmować postać takich objawów jak:
– przyspieszenie akcji serca
– obrzęki obwodowe
– niewydolność serca
Zaburzenie wynikające z układu krążenia może być przyczyną śmierci.
Objawy zespołu Korsakowa
Drugim elementem zespołu Wernickiego- Korsakowa jest zespół amnestyczny Korsakowa. Objawy w tym zespole wiążą się głównie z funkcjami psychicznymi człowieka. Najczęściej charakteryzują się przebiegiem przewlekłym i są trudniejsze do wyleczenia.
Naczelnym objawem w zespole Korsakowa są zaburzenia pamięci. Kiedy mówimy o zaburzeniach pamięci w tej chorobie, to mamy na myśli zaburzenia zarówno pamięci wstecznej jak i następczej. Jest to równoznaczne z tym, że u człowieka borykającego się z zespołem Korsakowa występuje niemożność przypominania sobie wydarzeń z przeszłości (zarówno tej dalekiej jak i bliskiej na przykład tego, co wydarzyło się wczoraj), oraz brak przyswajania sobie nowych informacji.
Dziury w pamięci zapełnia tak zwanymi konfabulacjami – czyli wymyślonymi wydarzeniami. Konfabulacji nie należy odbierać jako mówienia nieprawdy, czy celowego oszukiwania. Człowiek ten nie jest bowiem świadomy, że podaje fałszywe informacje. Jest przekonany, że wydarzenia, o których mówi miały miejsce.

Inną cechą zespołu Korsakowa są zaburzenia osobowości. Często spotykane są takie cechy jak: labilność emocjonalna, niedostosowanie zachowania do sytuacji, odhamowanie.
Leczenie zespołu Wernickiego- Korsakowa
Leczenie zespołu Wernickiego- Korsakowa na etapie ostrych dolegliwości zawsze kwalifikuje się do pobytu w szpitalu. Najpilniejsze jest uzupełnienie niedoboru witaminy B1. W związku z utrudnionym wchłanianiem, najczęściej witamina podawana jest w postaci zastrzyków domięśniowych. Powinno się również pamiętać o ograniczeniu w tym czasie podaży cukrów oraz o prawidłowym nawodnieniu. Kiedy ostre objawy zespołu niedoboru witaminy B1 ustąpią należy przewlekle ją uzupełniać suplementami oraz zachować całkowitą abstynencję. Niestety nie zawsze udaje się uzyskać całkowitą poprawę stanu zdrowia. Niektóre objawy psychiatryczne, szczególnie te, które zaliczają się do zespołu Korsakowa są nieuleczalne.
źródła zdjęć:
https://www.miod-malina.pl/zdjecia/witamina-b1.jpg
https://ocdn.eu/pulscms-transforms/1/MLIktkqTURBXy9jN2YxZWIzODEzNDI4NDgyOWU2OGM2NzIwYTI2MWU5MS5qcGVnk5U
D_3XNCEjNBKmTBc0DFM0BvJUH2TIvcHVsc2Ntcy9NREFfLzE0MGIxY2ZlN2YwYWM1MmVkYzAxMGQ3MDk3OGU4NGJlLnBuZwDCAA
Alkaloza metaboliczna
23 lipca, 2019 BlogCo to jest alkaloza metaboliczna?
Alkaloza metaboliczna zwana również zasadowicą metaboliczną lub nieoddechową należy do zaburzeń równowagi kwasowo- zasadowej. Równowaga ta to utrzymanie odpowiedniego stężenia jonów wodorowych w przestrzeni zewnątrz- i wewnątrzkomórkowej. Sprawia to, że komórki i narządy prawidłowo funkcjonują w organizmie. Wyznacznikiem, który wskazuje na stężenie jonów wodorowych jest pH krwi. Prawidłowo powinno ono wynosić około 7,35-7,45. Gdy pH jest większe od tej wartości mówi nam to o występowaniu zasadowicy (alkalozy), natomiast spadek pH świadczy o kwasicy.

Możemy rozdzielić kwasicę, jak i zasadowicę ze względu na mechanizm jej powstawania na oddechową i nieoddechową (metaboliczną). Zasadowica metaboliczna może zależeć od zwiększonej utraty jonów wodorowych, jak również od nadmiernego przyjmowania i zmniejszonego usuwania zasad, w tym jonów wodorowęglanowych.
Alkaloza metaboliczna – przyczyny
Do głównych przyczyn alkalozy metabolicznej należy utrata jonów wodorowych i chlorkowych z organizmu. Może się tak dziać na skutek wymiotów i biegunek drogą pokarmową, a także przez nerki na przykład w wyniku nadmiernego podania leków o działaniu moczopędnym.
Nie bez znaczenia jest hipowolemia czyli obniżenie objętości płynu zewnątrzkomórkowego. Efektem tego jest nadmierne wchłanianie jonów wodorowęglanowych w nerkach, a zatem rozwój zasadowicy.
Do utraty jonów wodoru przez nerki może dojść także w przypadku tak zwanej tubulopatii. W klasyfikacji medycznej należy ona do rzadkich chorób, które charakteryzują się zaburzeniem funkcji cewek nerkowych. Należą do nich między innymi zespół Barttera oraz zespół Gitelmana.
Alkaloza metaboliczna objawy
Objawy alkalozy metabolicznej są różne i mogą powodować obciążenie poszczególnych układów w różnym stopniu.
Jednym z wyróżników alkalozy metabolicznej są zaburzenia ze strony układu nerwowego. W związku z tym pacjenci mogą cierpieć na: zaburzenia świadomości, zaburzenia pamięci i koncentracji, psychozy, zaburzenia lękowe, zawroty głowy oraz parastezje.
Szczególnym zagrożeniem mogą być symptomy ze strony układu krążenia. Następstwem zaburzeń elektrolitowych mogą być zaburzenia rytmu serca. U chorych następują spadki ciśnienia tętniczego oraz spadek rzutu serca.
Skutkiem zaburzeń ze strony układu oddechowego jest niedobór tlenu we krwi czyli hipoksemia. Może się to wiązać z zaburzeniami pracy mięśni oddechowych.
Do innych objawów alkalozy należą: tężyczka czyli nadmierne skurcze mięśni spowodowane spadkiem poziomu wapnia w surowicy. Do skurczu szkieletowych mięśni kończyn mogą dołączyć tak zwane równoważniki tężyczki, które przybierają formę: skurczu naczyń mózgowych (następstwem tego jest przemijające niedokrwienie mózgu), skurczu naczyń wieńcowych (prowadzi to do objawów choroby niedokrwiennej serca), skurczu naczyń brzusznych (powoduje anginę brzuszną), a także skurczu naczyń obwodowych.
Alkaloza metaboliczna – powikłania i komplikacje
W przypadku nieleczenia możemy spotkać się z różnymi komplikacjami. Odmianę powikłania wyróżniamy na podstawie choroby prowadzącej do alkalozy. W przypadku współwystępowania ciężkich zaburzeń elektrolitowych możemy spotkać się z niebezpiecznymi dla życia zaburzeniami rytmu serca.

Hipowentylacja współistniejąca z zasadowicą metaboliczną może z kolei prowadzić do niedotlenienia ośrodkowego układu nerwowego. W trakcie trwania zasadowicy nieoddechowej pojawiają się działania kompensacyjne, których funkcją jest przywrócenie równowagi kwasowo- zasadowej. Towarzyszą temu procesowi płuca, które dzięki hipowentylacji zwiększają stężenie parcjalne dwutlenku węgla we krwi, oraz nerki, które pozbywają się nadmiaru wodorowęglanów.
Wartość pH krwi decyduje o rokowaniu. Wraz z jego wzrostem rokowanie pogarsza się. Przy wartości pH 7,65 śmiertelność osiąga około 80%.
Alkaloza metaboliczna- badania
Pierwszym badaniem, które wykonuje się w przypadku podejrzenia alkalozy metabolicznej jest gazometria krwi tętniczej. Badanie to polega na pobraniu krwi tętniczej – zazwyczaj z tętnicy udowej lub promieniowej. O alkalozie metabolicznej świadczy podwyższone pH – powyżej 7,45,oraz prawidłowe ciśnienie parcjalne dwutlenku węgla i zwiększony poziom wodorowęglanów. Jest to wówczas zasadowica metaboliczna niewyrównana. Efektem działania mechanizmów kompensacyjnych jest wzrost ciśnienia parcjalnego dwutlenku węgla, a w warunkach zasadowicy całkowicie wyrównanej do unormowania wartości pH.
Alkaloza metaboliczna – leczenie
W leczeniu alkalozy metabolicznej ważna jest walka z przyczynami leżącymi u źródła zachwiania równowagi kwasowo- zasadowej. Nieodzowne może się okazać odstawienie leków moczopędnych lub przeczyszczających. Pacjenci zmagający się z silnymi wymiotami i biegunkami powinni pamiętać o stosownym nawodnieniu- czyli płynoterapii. Kiedy stwierdzony zostaje niedobór potasu konieczne jest jego uzupełnienie.
Natomiast zaleca się aby osoby zdrowe trzymały się zasad prawidłowego żywienia, co może ustrzec je w przyszłości przed zachorowaniem na alkalozę metaboliczną.
źródła zdjęć:
https://szelazo.pl/wp-content/uploads/2018/10/zmęczenieanemia.jpg
https://img-3.fruugo.com/product/4/11/22127114_max.jpg
Choroba HALLERVORDENA
4 lipca, 2019 BlogNa czym polega choroba Hallervordena?
Choroba Hallervordena jest to zwyrodnienie układu nerwowego z namnożeniem się żelaza w mózgu. Jest rzadką, dziedziczną chorobą, której istotą jest neurologiczne, postępujące zaburzenie ruchowe. Ostatnio udało się znaleźć jedną z genetycznych przyczyn choroby, jednakże są jeszcze inne geny wywołujące tę chorobę, które nie zostały zidentyfikowane. U około 50% pacjentów zaobserwowano mutację genu PNAK 2, który bierze udział w metabolizowaniu witaminy B5. Cechą charakteryzującą wszystkie przypadki choroby jest gromadzenie się żelaza w mózgu wraz z postępującymi zaburzeniami ruchu. Pacjenci mogą przez dłuższe etapy czasu czuć się dobrze (sytuacja chorego może być ustabilizowana), po czym następuje remisja objawów. Oczywiście nie ma takich samych przypadków choroby, każdy jest indywidualny. Dzieje się tak dlatego, że genetyczne mutacje mogą się różnić w poszczególnych rodzinach.

Czynniki wpływające na intensyfikację symptomów choroby i na jej bardziej dynamiczny rozwój nie zostały poznane. Cechy wyróżniające tę chorobę i występujące u wszystkich pacjentów to: dystonia (anomalia w napięciu mięśniowym, torsje), sztywność mięśni i nagłe mimowolne skurcze mięśni (spastyczność). Wyróżnione cechy mogą stać się przyczyną problemów z chodzeniem, niezdarności, trudności w kontrolowaniu ruchów i problemów z mówieniem. Inną cechą łączącą te przypadki jest degeneracja siatkówki, która prowadzi do postępującej kurzej ślepoty. Niestety trzeba przygotować się na to, że objawy choroby postępują i są coraz silniejsze. Choroba różni się pod względem problemów jakie wywołuje. Ważne jest edukowanie rodziców dzieci,u których dopiero co zdiagnozowano tę chorobę, aby zdawali sobie sprawę z owej różnorodności objawów, którymi przejawia się to schorzenie. Istnienie wielu objawów nie jest równoznaczne z tym, że u każdego dziecka będą obecne wszystkie z nich lub, że będą one bardzo nasilone.
Jakie są objawy choroby Hallervordena?
Nerwowo- mięśniowe objawy powiązane z wszystkimi formami choroby Hallervordena:
– Choreoatetoza – jest położeniem, w którym pojawiają się mimowolne nagłe i nerwowe ruchy (pląsawica) występujące na przemian z stosunkowo wolnymi, wykręcającymi ciało ruchami (atetoza).
– Dystonia jest zaliczana do grupy zaburzeń mięśni gładkich, wywołujących ich kurczenie się, które mogą zmuszać pewne części ciała do niezwykłych i bolesnych ruchów oraz pozycji. Dystonia (mimowolne skurcze mięśni) oddziałuje również na mięśnie w ustach i gardle, co może być przyczyną słabej artykulacji i mamrotania (dysarthria), a także trudności z połykaniem. Postępująca dystonia w tych mięśniach, powoduje możliwą utratę mowy, jak również gryzienie języka.
– Blepharospasm – jest to upośledzenie mięśni powiek, którego konsekwencjami są nadmierne mruganie i mimowolne zamknięcie powiek.
– Spastyczność i sztywność mięśniowa – początkowo dotyka nóg. W późniejszym stadium rozwija się w ramionach, co wywołuje utratę kontroli nad ruchami ciała. Skurcze mięśni mogą powodować złamania kości (które nie są skutkiem traumy ani wypadku)
– Torticollis – bezwiedne kurczenia się z mięśni szyi, powodujące odbiegające od normy ruchy i pozycje głowy i szyi.
Jakie są rokowania w przypadku tej choroby?
Choroba Hallervordena jest postępowym niedowładem. Ma charakter nagłych wybuchów choroby, nie posuwa się do przodu w równym tempie. Okresy nagłego pogorszenia trwające przez odcinek czasu od jednego do dwóch miesięcy, przeplatają się ze stanami stabilizacji pomiędzy. Zaczynając się u dzieci choroba może rozwijać się szybciej. Chorzy nie mogą poruszać się o własnych siłach i potrzebują wózka inwalidzkiego, z uwagi na fakt rozwijającej się u nich dystonii i spastyczności. Przedwczesna śmierć jest możliwa w chorobie Hallervordena. Jednak długość życia pacjentów nie jest stała. Chorzy, którzy są pod stałą opieką lekarską mogą dożyć nawet do wieku dojrzałego. Powodem przedwczesnej śmierci jest zazwyczaj dystonia i ograniczone przełykanie, które może powodować zmniejszoną rację spożywanych posiłków i zapalenie płuc. Lepsze rokowania mają pacjenci, u których choroba pojawiła się w późniejszym wieku, choroba przebiega łagodniej, a co za tym idzie mogą oni dożyć do wieku dojrzałego.
Jak można rozpoznać chorobę?
Aby zdiagnozować chorobę Hallervordena należy wykonać badanie rezonansu magnetycznego. Jest to metoda obrazowa, która daje obszar do obserwacji charakterystycznego nagromadzenia się żelaza w pewnych obszarach mózgu (istota szara).
Choroba Hallervordena – leczenie
Nie ma uniwersalnego sposobu leczena tej choroby, polega ono głównie na łagodzeniu jej objawów. Leczenie może obejmować współpracę specjalistów takich jak: pediatra albo internista, neurolog, okulista i genetyk. Zespołowe wsparcie terapeutyczne powinno obejmować także: gimnastykę, fizjoterapię, hipnoterapię oraz masaże rozluźniające mięśnie.
źródła zdjęć:
https://s3.envato.com/files/244482792/preview.jpg
https://cdn.galleries.smcloud.net/t/galleries/gf-cDg9-YsRq-Lq8V_choroba-hallervordena-spatza-to-zwyrodnienie-ukladu-nerwowego-1920×1080-nocrop.jpg
Glejak mózgu
2 lipca, 2019 BlogCo to jest glejak mózgu?
Glejaki w terminologii medycznej należą do grupy nowotworów ośrodkowego układu nerwowego, które mają swój początek w komórkach glejowych. Glejaki mają różne postacie w obrębie komórek mózgu, w których mają swoje źródło (astrocyty, oligodentrocyty). Różnią się także stopniem agresywności.
Nowotwory złośliwe czyli glejaki, które mogą występować w każdym miejscu w obszarze ośrodkowego układu nerwowego, co wskazuje głównie na mózg, a rzadziej na rdzeń kręgowy. Glejaki wyróżniają się właściwością polegającą na lokalnym rozszerzaniu się w obrębie ośrodkowego układu nerwowego.
Nowotwory tego typu mogą pojawiać się u osób w każdym wieku, jednak najbardziej rozpowszechnione są u osób w 5. i 6. dekadzie życia.
Przyczyny glejaka
Nie znane jest pochodzenie tej choroby. Znaleziono co prawda kilka czynników ryzyka, które mogą zwiększać prawdopodobieństwo zachorowania na glejaka, choć nie zawsze okazują się one czynnikiem sprawczym. Czynniki ryzyka mogą mieć wpływ na zachorowanie, ale nigdy nie stanowią bezpośredniej przyczyny choroby.
Wśród czynników, które mogą zwiększyć ryzyko zachorowania można wymienić:
– tendencje rodzinne: występowanie glejaka wśród najbliższych krewnych (przynajmniej jeden przypadek w tej samej rodzinie) dwukrotnie zwiększa niebezpieczeństwo zachorowania
– zespoły genetyczne: niektóre wrodzone zespoły predestynują do większego niebezpieczeństwa zachorowania na glejaka głównie z powodu obecności jednej lub więcej mutacji genetycznych. Przykładowo są to zespoły: Cowden, Turcota, Lyncha, Li–Fraumeniego oraz
nerwiakowłókniakowatość typu I.
Rodzaje glejaków
Glejaki, po poddaniu badaniom histopatologicznym wyróżnia się ze względu na typy komórek nerwowych, z których się wywodzą (astrocyty, oligodendrocyty lub ependymocyty).
Istnieje również podział w skali od I do IV. W rozróżnieniu tym bierzemy pod uwagę szybkość wzrostu guza i jego agresywność.
– guzy I stopnia – występują one również u dzieci, dają najlepsze rokowania
– guzy II stopnia – (glejaki wysokozróżnicowane) należą do guzów wolno rosnących, naciekowych, wiążą się ze średnimi rokowaniami
– guzy III stopnia (anaplastyczne) i IV stopnia (glejaki wielopostaciowe) są agresywne o najmniej korzystnym rokowaniu.
Objawy glejaka
Może zaistnieć przypuszczenie o glejaku, gdy pojawiają się niepokojące objawy takie jak: zawroty głowy, zachwiania równowagi, napady padaczkowe, zmiany osobowości oraz wszelkiego rodzaju zaburzenia neurologiczne- w tym zaburzenia widzenia, mówienia, utrata siły mięśniowej, zmiana chodu. Objawy glejaka mogą również dawać o sobie znać pod postacią wzrostu ciśnienia w czaszce. Symptomami tego mogą być: bóle głowy, mdłości, senność, wymioty.
Glejak diagnoza
Przy rozpoznaniu glejaka lekarz kieruje na badanie rezonansu magnetycznego (MRI) mózgu. Zakres obrazowy tej metody pozwala nie tylko na wykrycie glejaka, ale także na określenie obszaru choroby.
W razie podejrzenia guza mózgu często najpierw stosuje się tomografię komputerową z użyciem środka kontrastowego.
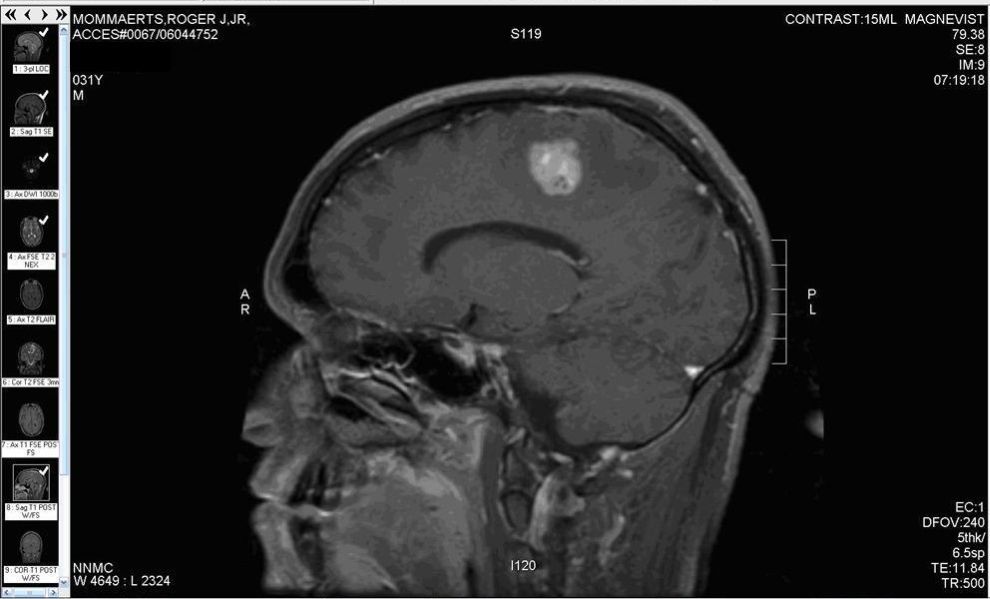
Należy również pobrać tkankę do badania histopatologicznego- podczas operacji chirurgicznej lub za pomocą biopsji. Badanie laboratoryjne tkanki ma za zadanie uprawomocnienie rozpoznania i określenie charakterystyki, podtypu guza, co stanowi podpowiedź co do sposobu leczenia.
Glejak leczenie
Podstawowym leczeniem glejaka jest zabieg chirurgiczny o możliwie jak najszerszym zakresie. Leczenie podjęte po operacji zależy od podtypu glejaka:

– glejak wysokozróżnicowany (stopień 1 i 2) u osób, u których możliwe jest w dużym stopniu ryzyko nawrotu choroby po operacji wdraża się radioterapię. Mniejsze znaczenie ma w leczeniu glejaków wysokozróżnicowanych chemioterapia stosuje się ją wówczas, gdy guz nie ma zalecenia do operacji, lub w przypadku guzów nawracających po radioterapii.
– glejak anaplastyczny (stopień 3) pooperacyjne leczenie glejaka anaplastycznego polega na zastisowaniu radioterapii a następnie chemioterapii.
– glejak wielopostaciowy (stopień 4) leczenie po opercji wymaga jednoczesnego stosowania chemioterapii i radioterapii (leczenie skojarzone)
źrodła zdjęć:
https://www.hellozdrowie.pl/wp-content/uploads/2019/01/glejak-wielopostaciowy-1140×760.jpg
https://glejak.com/wp-content/uploads/2013/10/glejak-mozgu-rak-mozgu.jpg
https://i.wpimg.pl/640×284/portal-abczdrowie.wpcdn.pl/imageCache/2018/11/22/98189108-m_c1e9.jpg
Przemijająca niepamięć ogólna
12 kwietnia, 2019 BlogCo to jest przemijająca niepamięć ogólna?
Przemijająca niepamięć ogólna (PNO) inaczej przemijająca amnezja globalna to krótkotrwałe i przemijające zaburzenia pamięci. Przebadano osoby w średnim i podeszłym wieku, których ogólny stan zdrowia był dobry, a nastąpiło u nich głębokie zaburzenie pamięci, trwające kilka godzin. Chorzy zapamiętywali podane im informacje tylko przez kilkadziesiąt sekund i w typowy sposób powtarzali te same pytania chcąc zorientować się w sytuacji. Do niepamięci następczej dołączała się różnej długości niepamięć wsteczna. Świadomość własnej osoby była zachowana.

Nie stwierdzono zaburzeń zmysłów, nie pojawiały się współwystępujące automatyzmy i ogniskowe objawy neurologiczne. Po kilku godzinach zapamiętywanie było przywrócone. Pozostawała głęboka pustka pamięciowa, za którą krył się okres zaburzeń. Statystycznie wiek chorych wynosił 62 lata, 90% chorych miało 59-70 lat. PNO rzadko występuje wśród osób młodych i jeśli wystąpi trzeba się liczyć z zachorowaniem na padaczkę. U 10- 20% osób, u których pojawiło się PNO, występowały ponowne incydenty niepamięci.
Przemijająca niepamięć ogólna -przyczyny
Patogeneza opisywanej choroby jest do tej pory niepoznana. Powstało kilka tez próbujących wyjaśnić jej przyczyny:
teoria zakrzepowo- zatorowa, która zakłada, że przemijająca niepamięć ogólna jest odmianą przejściowych ataków niedokrwiennych,
teoria padaczkowa charakteryzująca przemijającą niepamięć ogólną jako napad padaczkowy częściowy, albo jako zjawisko analogiczne do porażenia ponapadowego Todda,
teoria migrenowa według, której przyczyną PNO jest skurcz gałęzi tętnic kręgowo- podstawnych o mechanizmie migrenowym
Zaburzenia te wiążą się zawsze z strukturami wchodzącymi w skład kręgu Papeza, w zakresie którego znajdują się zakręty hipokampa, sklepienie, ciała suteczkowate, grzbietowo-przyśrodkowe jądro wzgórza i zakręty obręczy. Struktury te uczestniczą w przetwarzaniu sygnałów poruszających się w ich sieci neuronalnej (pamięć świeża) na trwałe makromolekularne struktury białkowe- engramy (pamięć trwała), gdzie ślady pamięciowe zostają utrwalone i zachowane.

Badacze głoszą, że uszkodzenie tych okolic powoduje niemożność zapamiętania nowych wrażeń. Można przypuszczać, że niepamięć wsteczna w PNO jest spowodowana nieprawidłowym funkcjonowaniem wymienionego wyżej kręgu neuronalnego, którego prawidłowa czynność jest konieczna dla zapobieżenia powstawaniu błędnych engramów pamięciowych. Wiąże się to przede wszystkim ze świeżymi wrażeniami pamięciowymi, dlatego niepamięć wsteczna jest ograniczona do zdarzeń ostatnich godzin, dni lub tygodni przed zachorowaniem.
Przemijająca niepamięć ogólna – objawy i rozpoznanie
Przejawia się jako utrata pamięci, która pojawia się po zadziałaniu znanych czynników. Przemijające zaburzenia pamięci mogą współwystępować z urazami głowy i szyi i mogą być spowodowane napadami padaczkowymi, przyjęciem niektórych leków lub mogą mieć podłoże psychogenne.
Zauważono utratę pamięci występującą po arteriografii tętnic kręgowych, szyjnych i wieńcowych.
Cechy odróżniające przejściową niepamięć towarzyszącą napadom padaczkowym od PNO to:
– częściowa niepamięć ataku
– występowanie amnezji wkrótce po przebudzeniu
– powtarzanie się epizodów zaburzeń pamięci
– niepamięć wsteczna nieproporcjonalnie duża w stosunku do następczej
– brak stereotypowego zadawania pytań z uczuciem lęku i zakłopotania
– ewidentna poprawa po wprowadzeniu leczenia przeciw padaczkowego
– krótki czas trwania niektórych ataków
– nieprawidłowy międzynapadowy zapis EEG
– występowanie automatyzmów lub okresów braku kontaktu w trakcie lub bezpośrednio przed amnezją
– występowanie napadów padaczkowych nizależnie od amnezji
Przemijająca niepamięć ogólna – rokowania
Choroba ta przebiega łagodnie. Właściwym temu zaburzeniu skutkiem jest kilku lub kilkunastogodzinna pustka pamięciowa. Mówiąc o wspomnianej luce pamięciowej mamy na myśli okres przed zachorowaniem i czas trwania samego epizodu.
Gorsze rokowania mają pacjenci z krótkimi lub nawracającymi incydentami choroby. Istnieje wówczas niebezpieczeństwo rozwoju w przeciągu 1 roku padaczki.
Z uwagi na fakt, że PNO ma łagodny charakter i przebieg nie istnieje konieczność leczenia. Chorzy powinni być jednak pod stałą opieką psychologiczną ponieważ zaburzenie to pojawia się u osób do tej pory zdrowych nagle i bez wyraźnej przyczyny.
źródła zdjęć:
https://i.iplsc.com/-/0001B3NLNE0VC5NU-C122-F4.jpg
.http://ambercare24.pl/wp-content/uploads/2017/07/511dt_150709_migraine_headache_brain_stroke_800x600-800×548.jpg
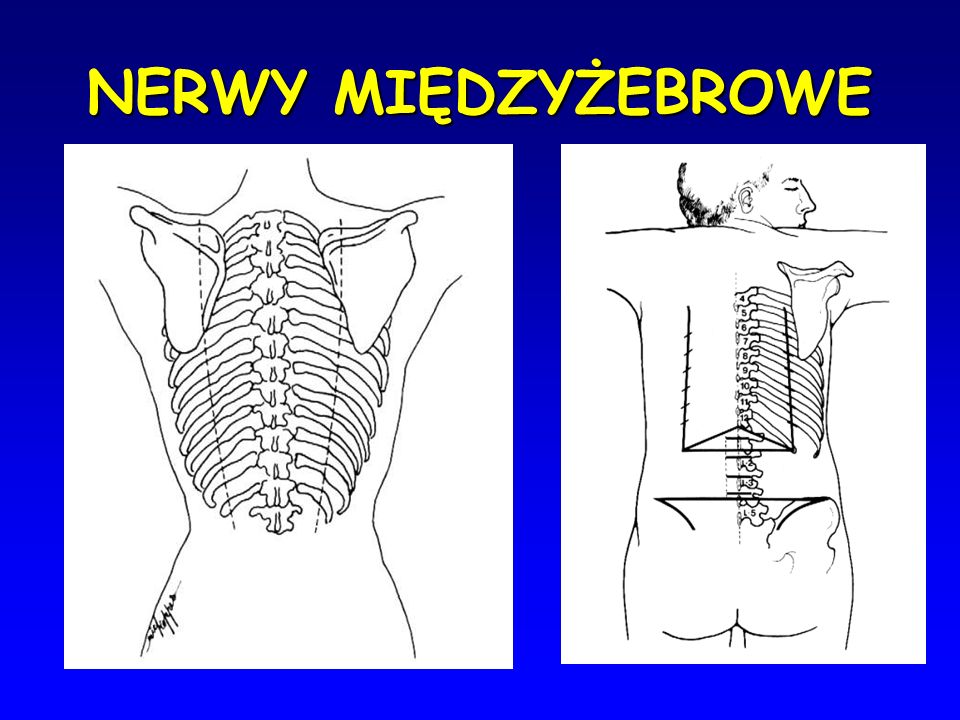
Nerwoból międzyżebrowy
28 marca, 2019 BlogCzym jest nerwoból międzyżebrowy?
Nerwoból międzyżebrowy inaczej neuralgia jest to przypadłość bólowa, umiejscowiona w okolicy unerwienia przez określone nerwy obwodowe. Jest efektem ich uszkodzenia. Bóle te mogą być odczuwalne jako rwące, szarpiące oraz ostre.
Nerwobóle międzyżebrowe są częstym powodem występowania bólu w klatce piersiowej. Ich źródłem jest uszkodzenie nerwów międzyżebrowych, które przebiegają między żebrami oraz unerwiają skórę klatki piersiowej i górnej części brzucha, a także mięśnie, opłucną i stawy.
Jakie są przyczyny występowania nerwobólu międzyżebrowego?
Nerwobóle pleców i klatki piersiowej mają różnorodne pochodzenie. Prawdopodobnymi przyczynami występowania bólu międzyżebrowego są:
– osteoporoza
– dyskopatia- choroby krążka międzykręgowego na przykład tak zwane wypadnięcie dysku
– skrzywienie kręgosłupa – skolioza
– guzowate zapalenie tętnic
– skurcze oraz zapalenie mięśni międzyżebrowych
– urazy klatki piersiowej
– choroby reumatyczne (toczeń rumieniowaty układowy, reumatoidalne zapalenie stawów)
– ucisk nerwów międzyżebrowych ze strony różnych procesów rozrostowych (łącznie z chorobami nowotworowymi)
– niedoczynność tarczycy
– cukrzyca
– choroby zakaźne (najczęściej półpasiec)
Objawy wypływające z uszkodzenia nerwów międzyżebrowych, mogą być również skutkiem długotrwałego pozostawania w jednej pozycji.
Nerwoból międzyżebrowy – jakich objawów możemy się spodziewać?
Nerwobóle międzyżebrowe są odczuwane jako niespodziewanie pojawiający się silny, rwący, kłujący, rozrywający ból między żebrami. Punkty objawów bólowych są takie same jak przebieg odpowiednich nerwów.
Nerwoból międzyżebrowy najczęściej jest zlokalizowany tylko z jednej strony, zdarza się jednak, że jest obustronny. Ból w okolicach żeber jest intensywniejszy przy kaszlu, wdechu, ruchach tułowia, kichaniu.
Chorzy odczuwają również ból przy dotyku. Powiększenie bólu może być spowodowane nawet przez tylko lekki dotyk wzdłuż przebiegu nerwów. Rozpiętość w czasie dolegliwości jest opisywana jako od kilku godzin do nawet kilku dni. Objawami współtowarzyszącymi mogą być: uczucie drętwienia, zaczerwienienie skóry, zaburzenia czucia w obszarze unerwienia przez dany nerw, czasami nasilona potliwość.
Nerwoból międzyżebrowy – co z tym robić?
W większości przypadków nerwoból nie jest ryzykowny dla zdrowia ponieważ ustępuje samoistnie w okresie kilku dni nie powodując żadnych groźnych powikłań. Kiedy dolegliwość nawraca, głównym założeniem leczenia jest usunięcie przyczyny lub leczenie choroby podstawowej, która jest źródłem bólu.
W fazie choroby, w której ból jest ostry głównie przeciwdziała się bólowi, stosując leki przeciwbólowe, a także środki zmniejszające napięcie mięśni.
Tymczasową ulgę może przynieść zastosowanie blokady z wyłączeniem funkcji nerwu ( taki sposób stosuje się tylko w niektórych przypadkach). Warto zwrócić uwagę na rolę witamin z grupy B szczególnie B12 i B6, które wspomagają regenerację uszkodzeń nerwów i odgrywają ważną rolę w prawidłowym funkcjonowaniu układu nerwowego. Istnieją również domowe sposoby leczenia takie jak ziołolecznictwo.
Aby zmniejszyć dolegliwości bólowe stosuje się również zabiegi fizjoterapeutyczne, takie jak:
– przezskórna stymulacja nerwów
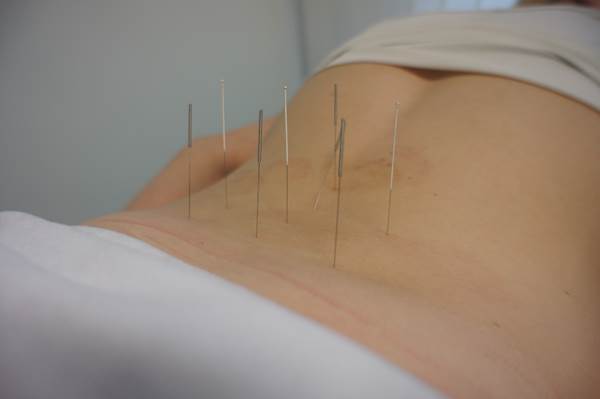
– akupunktura
– jonoforeza (jej mechanizm polega na wprowadzeniu miejscowo leku przy pomocy prądu stałego)
– akupresura (pobudzanie zakończeń nerwowych przez miejscowy ucisk)
Niekiedy w neuralgiach odwołuje się do leczenia chirurgicznego na korzeniach nerwowych, pniu lub zwojach objętych schorzeniem.
źródła zdjęć:
http://akupunktura-arkadia.pl/wp-content/uploads/2015/04/neuralgia.jpg
http://www.dobrylekarz.info/files/node_images/aku_plecy.jpg
https://slideplayer.pl/slide/8573843/25/images/67/NERWY+MIĘDZYŻEBROWE
Krwotok podpajęczynówkowy
14 marca, 2019 BlogCo to jest krwotok podpajęczynówkowy?
Krwotok podpajęczynówkowy to przypadłość, w której występuje nieprawidłowość przepływu krwi. Krew przedostaje się do strefy między oponą pajęczą a miękką (przestrzeń podpajęczynówkowa), gdzie znajduje się płyn mózgowo- rdzeniowy.
Każdego roku w Polsce statystyki pokazują nowe zachorowania. Jest ich około 3 tysięcy, a jedna czwarta kończy się śmiercią.
Przyczyny krwotoku podpajęczynówkowego
Krwotok podpajęczynówkowy może być wynikiem:
– pęknięcia tętniaka (najczęściej)
– naczyniaka mózgu (rzadko)
– obecności skazy krwotocznej
– przebytego urazu głowy
Krwotok podpajęczynówkowy – objawy
Krwotok podpajęczynówkowy może zaskoczyć pacjenta nagłym początkiem choroby. Może wystąpić nawet gdy chory czuje się dobrze i zdrowo. Niektórym chorym na kilka dni lub tygodni przed pojawieniem się krwotoku może doskwierać ból głowy. Bóle te nie wyróżniają się jednak niczym szczególnym, co mogło by świadczyć o krwotoku.
Silne bóle głowy pojawiają się czasami w następujących okolicznościach, które mogą świadczyć o podwyższonym ciśnieniem tętniczym:
– kaszel
– emocje
– oddawanie stolca
– aktywność fizyczna
Jednak w większości przypadków bóle nie są powiązane z ciśnieniem tętniczym.
Ból głowy eskaluje przy każdym ruchu. Z bólem wiążą się często nudności i wymioty oraz dłużej lub krócej trwająca utrata przytomności. Rzadko pojawiają się drgawki, zaburzenia psychiczne lub porażenia ruchów gałek ocznych.

Przy silnych bólach głowy utracie na długi czas przytomności i innych objawach świadczących o uszkodzeniu mózgu – różnicuje się stopień ciężkości choroby. Wygląda on następująco: od niewielkiego (lekkie bóle głowy bez utraty przytomności) do skrajnie ciężkiego (pełna śpiączka z porażeniem kończyn).
Stan pacjenta może być niestabilny i ulegać gwałtownym zmianom. W ciągu pierwszych kilkunastu dni pogorszenie stanu zdrowia może być następstwem:
– ponownego krwawienia, do którego dochodzi u 25% chorych
– powikłań takich jak obrzęk mózgu bądź skurcz tętnic mózgowych powodujących niedokrwienie
Jeżeli przypuszcza się wystąpienie krwotoku podpajęczynówkowego należy niezwłocznie przetransportować chorego do szpitala, w którym jest specjalistyczny sprzęt diagnostyczny.

Krwotok podpajęczynówkowy – diagnoza
Aby trafnie rozpoznać krwotok podpajęczynówkowy należy wykonać badania tomografii komputerowej. Daje to możliwość wykrycia wynaczynionej krwi, a także ułatwia przybliżyć ocenę wynaczynionej krwi oraz pozwala określić ewentualną przyczynę krwawienia. Wykazać krwotok podpajęczynówkowy może również badanie płynu mózgowo- rdzeniowego, które sprawdza obecność domieszek krwi. Metodą tą bada się gdy nie ma możliwości wykonania tomografii komputerowej.
Krwotok podpajęczynówkowy – leczenie
Pacjent, u którego zdiagnozowano krwotok podpajęczynówkowy powinien przyjąć pozycję leżącą. Jeśli udało się uniknąć powikłań chory powinien leżeć unieruchomiony przez cztery tygodnie od momentu wystąpienia krwawienia. Kiedy lekarz stwierdzi tętniaka konieczna może być operacja, która ma za zadanie zabezpieczenie pacjenta przed kolejnym krwawieniem z tętniaka. Zabieg chirurgiczny powinien być wykonany niezwłocznie aby uchronić pacjenta przed kolejnym konsekwencjami (nawrót krwawienia).
źródła zdjęć:
- biomedical.pl/4_3/400/ce61ec922c5d07c101ab1d512ab517dd.jpg
- https://slideplayer.pl/slide/836340/2/images/7/slide/836340/2/images/7/Powikłania+Powtórne+krwawienie+(ryzyko+większe+w+ciągu+doby+od+pęknięcia+tętniaka).jpg
- https://zdrowie.tvn.pl/media/cache/content_thumbnail_small/xadobestock-70370388-jpeg.jpeg.pagespeed.ic.sya-kg4vlX.jpg
Padaczka
28 lutego, 2019 BlogCo to jest padaczka?
Padaczka, inaczej epilepsja, należy do chorób neurologicznych. Jest efektem chwilowej niesprawności mózgu, która polega na nagłych i napadowych wyładowaniach wewnątrz komórek nerwowych.
Charakterystycznym symptomami epilepsji są ataki silnych wstrząsów związane z utratą świadomości. O padaczce możemy mówić, że jest to zespół symptomów psychicznych wegetatywnych i somatycznych, które występują na skutek zmian morfologicznych i metabolicznych w mózgu.
Padaczka jest chorobą mózgu, w której zaburzone jest funkcjonowanie pewnych komórek nerwowych umiejscowionych w mózgu. Występowanie padaczki jest związane ze zmienioną reaktywnością lub stanem fizjologicznym części lub całości mózgu. Należy zwrócić uwagę, że każde niespodziewane, a nawet krótkotrwałe zaburzenie układu nerwowego, które występuje bez wyraźnej przyczyny może świadczyć o padaczce.
Przyczyny padaczki
Etiologia padaczki nie jest jednoznaczna. Padaczki nie da się rozpoznać u prawie 65% pacjentów. Najczęstszą przyczyną tej choroby są urazy głowy-stosunkowo 20% wszystkich przypadków. Mężczyźni stanowią grupę, u której epilepsję diagnozuje się znacznie częściej niż u kobiet.
U podłoża padaczki mogą leżeć takie przyczyny jak:
-udar
-toksyczno-metaboliczne uszkodzenie tkanki mózgowej
-nowotwór
-zapalenie mózgu i opon mózgowych
-uwarunkowania genetyczne (najczęściej dotyczą wieku dziecięcego)
-krwotok podpajęczynówkowy

Przyczyną padaczki może być również pojawiający się już w okresie okołoporodowym lub na późniejszym etapie życia uraz mózgu. Uraz ten najczęściej ma postać uszkodzenia, a u ludzi starszych niedokrwienia mózgu. Kiedy przyczyny padaczki są nierozpoznane, jak u większości dzieci, mówimy wówczas o padaczce idiopatycznej. U osoby dorosłej padaczka jest najczęściej wynikiem innej choroby, lub uzależnienia od alkoholu.
Objawy padaczki
Nie do końca prawdziwe jest utożsamianie padaczki z drgawkami i utratą przytomności. Ocenia się, że prawie 60% napadów padaczkowych to napady drgawkowe w tym 2/3 to napady ogniskowe, a 1/3 uogólnione. 40% wszystkich napadów padaczkowych to napady bez drgawkowe.
Gdy mowa jest o napadzie grand mal czyli napadzie toniczno-klonicznym, pojawiają się następujące objawy:
– utrata przytomności
-wyprężenie ciała
-następnie drgawki
-sinica
-“piana z ust”
-przygryzienie języka
-niekiedy bezwiedne oddanie moczu
Czas trwania takiego napadu wynosi od kilkunastu sekund do 3 minut. W stanie po-napadowym pacjent może odczuwać zmęczenie, senność, ból mięśni i ból głowy.
Drgawki kończyn górnych rzadziej dolnych, bez utraty świadomości mogą świadczyć o objawach napadu mioklonicznego.
Osobną grupę napadów padaczkowych stanowią napady nieświadomości, które częściej spotykane są u dzieci. Chory jest jakby zamyślony, wyłączony, nie reaguje na kierowane do niego słowa. Dopiero po kilku, kilkunastu sekundach wraca do rzeczywistości i może wykonywać przerwaną pracę.
Podczas napadu częściowego złożonego pacjent nie ma kontaktu z rzeczywistością, jest “nieobecny” przez około 2-3 minuty. Chory może mieć wówczas otwarte oczy, mogą być zauważalne tzw. automatyzmy, czyli czynności wykonywane automatycznie (np. mlaskanie, przełykanie śliny, skubanie ubrania, rozpinanie guzików).
Szacuje się, że u około 6% cierpiących na padaczkę choroba wywołana jest przez czynniki zewnętrzne np. migające światła, czy nagłe dźwięki.
Innym zagrożeniem jest wystąpienie po padaczce porażenia Todda. Występuje ono u około 13% chorych i może zwiększać ryzyko kolejnego napadu.
Leczenie padaczki
Leczenie ma na celu wdrożenie pacjenta do normalnego funkcjonowania. Efektem terapii ma być złagodzenie napadów lub spowodowanie ich całkowitego ustąpienia.
Istnieją dwa sposoby działania preparatów przeciwpadaczkowych:
-podnoszący próg drgawkowy
-działający poprzez ograniczanie rozprzestrzeniania się odogniskowych wyładowań na inne obszary mózgu dzięki temu zapobiegając wtórnemu uogólnionemu wyładowaniu, które charakteryzuje się uogólnionymi drgawkami toniczno-klonicznymi.

Lek powinien być indywidualnie dopasowany przez lekarza do schorzenia pacjenta to znaczy do rodzaju ataku drgawek. Jeśli jeden lek nie pomaga stosuje się drugi. Pacjent powinien przyjmować leki według ustalonego harmonogramu to znaczy o stałych porach i w określonych dawkach. Chory poddany leczeniu farmakologicznemu powinien okresowo wykonywać badania krwi najlepiej co pół roku. U niektórych pacjentów, którzy nie reagują na leczenie farmakologiczne konieczne jest wdrożenie leczenia neurochirurgicznego. Aby zmniejszyć częstotliwość i charakter napadów padaczkowych wykonuje się zabieg na tkance mózgowej.
Gdy tolerancja leków jest dobra i gdy podczas ich stosowania nie występują napady, chory może prowadzić normalne życie osobiste i zawodowe.
źródła zdjęć:
https://szczepienia.wybudzeni.com/wp-content/uploads/2018/07/Padaczka-po-szczepieniu_.jpg
https://www.medicover.pl/Data/Thumbs/storage_files/2018/4/12/eb143257-8fcf-45ec-a381-bfeea5b1c880/05da38b2-e0e7-4874-897f-eae240611e5f_cropped.jpg
https://www.rodzice.pl/wp-content/uploads/2018/07/epilepsja-u-dzieci.jpg
Objaw Raynauda
20 lutego, 2019 BlogCo to jest objaw Raynauda?
Objaw Raynauda to dolegliwość, której głównym objawem jest marznięcie nosa i małżowin usznych oraz drętwienie palców rąk i stóp. Charakterystyczny dla tej choroby jest nadmierny skurcz naczyń krwionośnych, który jest spowodowany stresem lub obniżoną temperaturą otoczenia.
Przyczyny tej przypadłości naczynioworuchowej są nieznane. Istotą tej choroby jest nagłe zblednięcie, następnie zsinienie i zaczerwienienie palców rąk, stóp rzadko nosa oraz uszu, które wiąże się z bólem i zdrętwieniem. Dolegliwość tą można określić jako pierwotną czyli choroba Raynauda, oraz wtórną czyli towarzyszącą innym chorobom- nazywaną zespołem Raynauda.
Choroba Raynauda- objawy
Pacjenci z chorobą Raynauda zazwyczaj zaliczają się do grupy wiekowej między 15. a 45. rokiem życia. Charakterystycznym objawem jest zblednięcie palców z uczuciem ich mrowienia pod wpływem zimna lub stresu. Kolejnym objawem jest ich sinienie i drętwienie, a po pewnym okresie czasu następuje zaczerwienienie z uczuciem bólu. Najczęściej dotyczy to palców rąk a często także palców stóp. Ponadto objaw może się pojawić w obszarze małżowin usznych, języka, nosa i warg. W niektórych przypadkach może dojść do wytworzenia się owrzodzeń opuszków palców, a nawet ich martwicy.
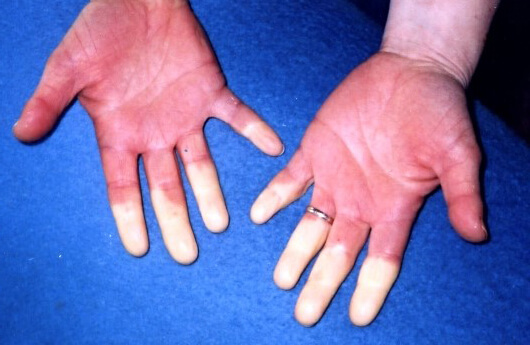
Zmiany zabarwienia, które są obecne w zespole Raynauda są dobrze odgraniczone, a także zróżnicowane- dotykają jednego lub więcej palców. U chorych można zaobserwować:
– blednięcie– jest ono przypadłością, która jest klasyczna dla fazy niedokrwiennej, jest efektem skurczu tętniczek w okolicy palców.
– sinica– upośledzenie prawidłowego krwawienia jest drogą do rozszerzenia żył i włośniczek, w efekcie odtlenowana krew zalega w naczyniach
– przekrwienie– występuje w czasie ogrzewania na skutek zaniknięcia skurczu tętnic palców i podniesienia poziomu przepływu krwi przez tętniczki i naczynia włosowate
Po wyeliminowaniu przypuszczeń wtórnych przyczyn objawu Raynauda mówimy o chorobie Raynauda. Warto wspomnieć, że połowa pacjentów z objawem Raynauda cierpi na chorobę Raynauda. W toku choroby zaatakowane zostają palce rąk. W początkowej fazie choroba może zająć jeden lub dwa opuszki palców, z biegiem czasu może zaatakować cały palec, a nawet wszystkie palce. Dla pewnych grup chorób charakterystyczne jest zgrubienie tkanki podskórnej w miejscu palców. Specjaliści twierdzą, że objaw Raynauda wykazuje łagodniejszy przebieg u osób cierpiących na chorobę.
Choroba Raynauda – przyczyny
Choroba i objaw Raynauda są spotykane w następujących dolegliwościach:
– toczniu rumieniowatym układowym
– reumatoidalnym zapaleniu stawów
– mieszanej chorobie tkanki łącznej
– zapaleniu wielomięśniowym i skórno- mięśniowym
– miażdżycy zarostowej kończyn
– ziarniniaku Wegenera
– chorobie Behçeta
– guzkowym zapaleniu tętnic
– twardzinie układowej
– zaburzeniach w składzie krwi
– zakrzepowo-zarostowym zapaleniu naczyń
– zaburzeniach w składzie krwi
W grupie ryzyka zachorowania na chorobę Raynauda są też osoby, u których wykryto mononukleozę zakaźną, zapalenie wsierdzia, chorobę z Lyme oraz wirusowe zapalenie wątroby typu B i C. Choroba Raynauda może wystąpić również u osób, które przyjmują niektóre leki kardiolgiczne, preparaty immunosupresyjne oraz doustne środki antykoncepcyjne. Duża zachorowalność występuje również wśród pracowników, w których zawodzie narażeni są na kontakt z metalami ciężkimi takimi jak: ołów i tal, a także na chlorek winylu.
Choroba Raynauda – rozpoznanie
W celu zdiagnozowania choroby Raynauda lekarz zbiera na początku informacje od chorego. Ma to formę wywiadu. Stosuje się również badania przedmiotowe oraz badania dodatkowe. Stwierdzenie objawów klinicznych chorób, w przebiegu których obecny jest objaw Raynauda, jest podstawą do rozpoznania zespołu Raynauda.
Ustalenie diagnozy jest ważne dla osób znajdujących się w grupie ryzyka rozwoju zespołu Raynauda. Do grupy tej zaliczają się osoby, u których objaw Raynauda wystąpił przed 30 rokiem życia oraz wszyscy, u których wykryto zmiany troficzne (owrzodzenie, martwica) w okolicy opuszek palców oraz chorzy na układowe choroby tkanki łącznej.
U pacjentów, u których możemy zaobserwować nagłe blednięcie palców u rąk i stóp, na skutek przeżywania silnych emocji lub uczucia zimna, wykonuje się badanie określane jako próba prowokacyjna. Próba ta polega na zanurzeniu na kilka minut w zimnej wodzie rąk lub stóp chorego lub włożeniu ich pod strumień zimnej wody. Oprócz tego należy wykonać badania krwi- jest to konieczne do stwierdzenia, co jest przyczyną objawu Raynauda. Jeżeli wynik badań jest pozytywny i dołączają się do tego objawy może to świadczyć o występowaniu zespołu Raynauda.
Leczenie objawu Raynauda
U większości chorych z objawem Raynauda terapia nie jest konieczna. Pacjenci z postacią wtórną choroby powinni być poddani leczeniu, jednak rzadko leczenie to bywa skuteczne. Terapia zespołu Raynauda ma za zadanie leczenie choroby podstawowej oraz objawów skurczu naczyń. Na pierwszym planie znajduje się profilaktyka. Dlatego lekarz powinien przekazać pacjentowi podstawowe informacje na temat choroby i sposobów jej zapobiegania. Najważniejsza jest zmiana nawyków chorego jak na przykład: rzucenie palenia, unikanie ekspozycji na zimno, odstawienie leków antykoncepcyjnych i preparatów powodujących skurcz naczyń krwionośnych oraz ograniczenie picia napojów zawierających kofeinę.
Farmakoterapię stosuje się wówczas, gdy choroba ma ciężki przebieg oraz gdy zawiodły inne środki doraźne. Wówczas stosuje się:
– blokety kanałów wapniowych, szczególnie zmniejszające objawy zespołu Raynauda, np. felodypina, nifedypina, isradypina oraz amlodypina;
– antagoniści postsynaptycznych receptorów α1-adrenergicznych – skuteczne są doksazosyna, prazosyna oraz terazosyna;
– preparaty sympatykolityczne w postaci pentoksybenzaminy, guanetydyny oraz metyldopy.
U pacjentów, u których organizm nie odpowiada na leczenie farmakologiczne przeprowadza się sympatekromię palców. Zabieg wygląda następująco: niszczy się nerw współczulny układu nerwowego, który zaopatrują naczynia krwionośne.
źródła zdjęć:

